
【题目】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
①A和B所属周期数之差为___________
②A和B的核电荷数之差为____________(用含m、n的代数式表示)
③B和A的族序数之差为______________(用含m、n的代数式表示)
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。回答下列问题:
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________;当B在A的下一周期时,B的原子序数为______________;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________当B在A的下一周期时,B的原子序数为______________。
(3)某粒子的结构示意图为: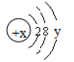 试回答:
试回答:
①当x-y=10时,该粒子为________(填“原子”或“阳离子”“阴离子”)
②当y=8时,该粒子可能是(写名称):_______、________、_______、_______、_______。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式________________。
【答案】1 m+n 8-n-m x-n x+m x-m x+n 原子 氩原子 氯离子 硫离子 钾离子 钙离子) Al(OH)3+3H+=Al3++3H2O
【解析】
(1)①因Am+和Bn-核外电子排布相同,故A原子比B原子多一个电子层,故二者的周期数之差为1,故答案为:1;
②电子排布相同,则电子数相同,即ZA-m=ZB+n,则ZA-ZB=m+n,故答案为:m+n;
③B的负价为-n,则最高正价为8-n,即B的族序数为8-n,而A的族序数为m,B和A的族序数之差为8-n-m,故答案为:8-n-m;
(2)①A、B同在ⅠA族,当B在A的上一周期时,B和A的原子序数之差恰好为B所在周期的元素种类数,则B的原子序数为x-n;当B在A的下一周期时,A和B的原子序数之差恰好为A所在周期的元素种类数,则B的原子序数为x+m,故答案为:x-n;x+m;
②A、B同在ⅦA族时,A、B原子序数之差恰好为相邻两周期下一周期的元素种类数,与A、B同在ⅠA族相反,如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为x-m,当B在A的下一周期时,B的原子序数为 x+n,故答案为:x-m;x+n;
(3)①当x-y=10时,核内质子数为x,核外电子数为2+8+y,两者相等,所以该粒子为原子,故答案为:原子;
②当y=8时,该微粒的核外电子数为18,而离子中核内质子数不等于核外电子数,则该粒子的核内质子数为:20、19、18、17、16等,所以这些粒子为氩原子、氯离子、硫离子、钾离子、钙离子,故答案为:氩原子;氯离子;硫离子;钾离子;钙离子;
③y=3与y=7的元素最高价氧化物对应水化物分别为Al(OH)3和HClO4,反应离子方程式为Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O。


科目:高中化学 来源: 题型:
【题目】有机化合物X、Y、A、B、C、D、E、F、G之间的转化关系如图所示。
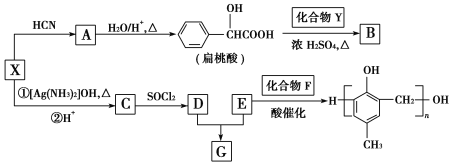
已知:①![]()
②![]() (R、R'代表烃基)
(R、R'代表烃基)
③X在催化剂作用下可与H2反应生成化合物Y;
④化合物F的核磁共振氢谱图中只有一个吸收峰。
请回答下列问题:
(1)X的含氧官能团的名称是________________________,X与HCN反应生成A的反应类型是_______________________。
(2)酯类化合物B的分子式是C15H14O3,其结构简式是__________________________。
(3)X发生银镜反应的化学方程式是:________________________。
(4)G在NaOH溶液中发生水解反应的化学方程式是_______________________。
(5)![]() 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。满足上述条件的同分异构体共有________种(不考虑立体异构)。
的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。满足上述条件的同分异构体共有________种(不考虑立体异构)。
(6)写出以C2H5OH为原料合成乳酸(![]() )的路线(其他试剂任选)。________________________________________________________________________。
)的路线(其他试剂任选)。________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为 1∶2 的是 ( )
A.3S+6NaOH= 2Na2S+ Na2SO3+3H2O
B.2 CH3COOH+Ca(ClO)2=2HClO+Ca(CH3COO)2
C.I2+2NaClO3=2NaIO3+Cl2
D.4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3 和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反 应的化学方程式为 2 KClO3 + 4HCl(浓) = 2 KCl + 2ClO2↑ + Cl2↑ + 2H2O。
(1)该反应的氧化产物是_____(填化学式)。
(2)在反应中浓盐酸表现出来的性质是_____(填字母)。
A.只有还原性 B.只有氧化性 C.还原性和酸性 D.氧化性和酸性
(3)若该反应产生 2.24 L(标准状况)ClO2,则转移电子的物质的量为_____。
(4)Cl2、H2O2、ClO2(还原产物为 Cl-)、O3(1 mol O3 转化为 1 mol O2 和 1 mol H2O)等物质常 被用作消毒剂。等物质的量的上述物质消毒效率最高的是_____(填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。充电时总反应为LiAO2 + nC = Li1-xAO2 + LixCn(0<x<1),工作原理如下图所示,则以下说法正确的是( )

A. 放电时Ni元素最先失去电子
B. 放电时电子从a电极由导线移向b电极
C. 充电时的阳极反应式为LiAO2 - xe-= Li1-xAO2 + xLi+
D. 充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )

A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2的导电能力之和大于HA的
C.b点的混合溶液pH大于7
D.c点的混合溶液中,c(Na+)>c(OH)>c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子的浓度变化如图所示(第一次平衡时c(I-)=2×10-3mol·L-1,c(Pb2+)=1×10-3mol·L-1),下列说法不正确的是

A.常温下,PbI2的Ksp=4×10-9
B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度减小,Pb2+浓度不变
C.T时刻可能向溶液中加入了KI固体,Ksp不变
D.常温下Ksp(PbS)=8×10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)反应的化学平衡常数为5×1018
PbS(s)+2I-(aq)反应的化学平衡常数为5×1018
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下Cu能与Fe3+发生反应:Cu+2Fe3+=Cu2++2Fe2+现将铜粉与二氧化二铁的混合物22.4g加入到1mol/L的H2SO4溶液中进行反应。
(1)若固体恰好溶解,消耗硫酸的体积为V,则V的取值范围是_______。
(2)若硫酸溶液过量,反应后溶液的体积为1L,测得此溶液中Fe2+的浓度为0.1mol/L,则混合物中含铜_______g或_______g(只需写出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
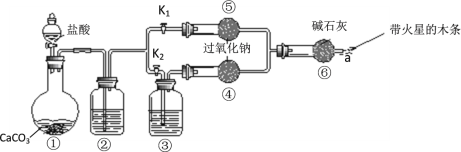
(装置分析)
(1)装置①中反应的离子方程式是___________;
(2)装置②中的试剂是______(填字母),装置③中的试剂是_________(填字母);
a 饱和NaHCO3溶液 b 饱和Na2CO3溶液 c 浓H2SO4 d NaOH溶液
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
步骤1中_____________,步骤2中_____________;
(4)步骤2中过氧化钠跟二氧化碳反应的化学方程式是_______________;
(实验反思)
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应” 。其理由是____________;
(6)需要补充的实验操作是:取⑤中反应后的少量固体,______________;
(测定实验)测定反应后⑤中固体CO32-的质量分数
(7)将反应后⑤中固体,称量质量为ag。将ag固体溶于水,加入__________(填“BaCl2”或“CaCl2”)溶液,与未选物质相比的优点是___________。将生成的沉淀过滤、洗涤、干燥、称量,得固体质量为bg,计算质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com