
| 溶质的质量 |
| 溶剂的质量 |
| 18.8g |
| 50g+18.8g |
| 50g+18.8g |
| 1200g/L |
| 18.8g |
| 188g/mol |
| n |
| V |
| 溶质的质量 |
| 溶剂的质量 |
| 18.8g |
| 50g |
| 18.8g |
| 50g+18.8g |
| 50g+18.8g |
| 1200g/L |
| 18.8g |
| 188g/mol |
| n |
| V |
| 0.1mol |
| 0.057L |


科目:高中化学 来源: 题型:
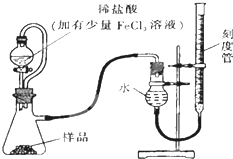 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.查看答案和解析>>
科目:高中化学 来源: 题型:
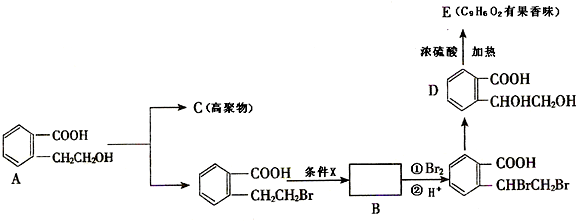
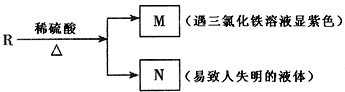
查看答案和解析>>
科目:高中化学 来源: 题型:

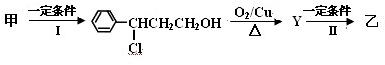
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴乙烷与NaOH醇溶液共热 |
| B、一氯甲烷与NaOH醇溶液共热 |
| C、溴乙烷与NaOH水溶液共热 |
| D、乙醇与浓硫酸共热至170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,AgCl的溶解度小于Ag2S的溶解度 |
| B、在25℃的AgNO3溶液中,AgCl的溶解度、Ksp均减小 |
| C、25℃时,在AgCl悬浊液中加入0.1mol?L-1 Na2S溶液,搅拌,生成Ag2S沉淀 |
| D、若取0.144g的AgCl放入100mL水中(忽略溶液体积的变化),则溶液中c(Cl-)=1.0×10-2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 24.01 |
| 2 | 25.00mL | 0.70 | 24.71 |
| 3 | 25.00mL | 0.20 | 24.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com