
 BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。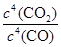
 Fe(OH)3+3H+,加入ZnCO3与H+反应,使水解平衡向右移动,得到Fe(OH)3沉淀。
Fe(OH)3+3H+,加入ZnCO3与H+反应,使水解平衡向右移动,得到Fe(OH)3沉淀。

科目:高中化学 来源:不详 题型:单选题
| A.观察氯化钾溶液没有颜色,表明溶液中的K+无色 |
| B.在氯化钾溶液中加入适量锌粉振荡,静置后未见明显变化,表明锌与K+不反应 |
| C.在高锰酸钾溶液中加入适量锌粉、振荡、静置后紫红色褪去,表明MnO4-为紫红色 |
| D.将高锰酸钾晶体加热分解,所得的固体质量减轻 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
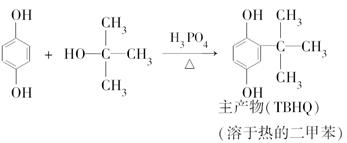
 丁醇,查阅资料得知一条合成路线:
丁醇,查阅资料得知一条合成路线: CH2+CO+H2
CH2+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO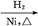 CH3CH2CH2CH2OH;
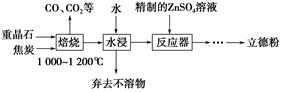
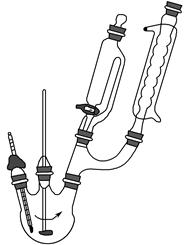
CH3CH2CH2CH2OH;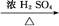 CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。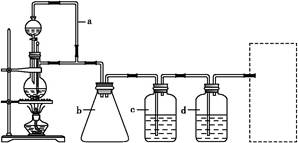
 丙醇,从中选择合适的试剂制备氢气、丙烯,写出化学反应方程式: , 。
丙醇,从中选择合适的试剂制备氢气、丙烯,写出化学反应方程式: , 。  丁醇粗品。为纯化1
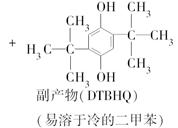
丁醇粗品。为纯化1 丁醇,该小组查阅文献得知:①R—CHO+NaHSO3(饱和)
丁醇,该小组查阅文献得知:①R—CHO+NaHSO3(饱和)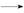 RCH(OH)SO3Na↓;②沸点:乙醚34℃,1
RCH(OH)SO3Na↓;②沸点:乙醚34℃,1 丁醇 118℃,并设计出如下提纯路线:
丁醇 118℃,并设计出如下提纯路线: 滤液
滤液
 有机层
有机层 1
1 丁醇、乙醚
丁醇、乙醚 纯品
纯品查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.检验某溶液中是否含有SO42-的方法是取少量该溶液加入BaCl2溶液,再加入稀硝酸 |
| B.用KMnO4酸性溶液可鉴别CH3CH=CHCH3和CH3CH2CH2CH2CH3 |
| C.用酚酞溶液或品红溶液均可鉴别NH3和SO2气体 |
| D.取工业有机废水(无色),滴加数滴FeCl3溶液,溶液变紫色,说明此废水中含酚类物质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定条件下可以用H2除去乙烷中混有的乙烯 |
| B.苯和四氯化碳都能萃取溴水中的溴 |
| C.乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法分离 |
| D.甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
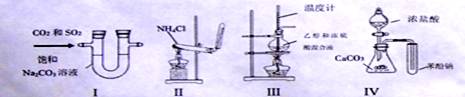
| A.用装置I除去CO2中的SO2 | B.实验室用装置II制备NH3 |
| C.用装置III制备乙烯 | D.装置IV比较酸性H2CO3>苯酚 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
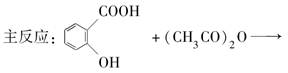
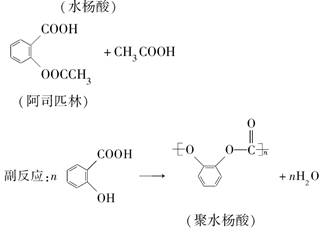
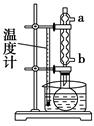
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 物质 | 杂质 | 试剂 | 主要操作 |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | NaHCO3 | NH4Cl | — | 加热 |
| C | 铁粉 | 铜粉 | 稀硫酸 | 过滤 |
| D | 甲烷 | 乙烯 | 溴水 | 蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com