
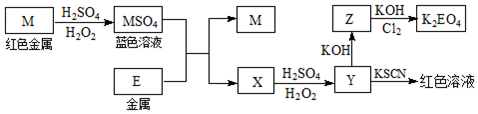
分析 M是红色金属,M和稀硫酸、双氧水反应生成硫酸盐,溶液呈蓝色,则M为Cu,MSO4为CuSO4;金属E和硫酸铜反应生成Cu和X,X和稀硫酸、双氧水反应生成Y,Y和KSCN溶液混合得到红色溶液,则Y为Fe2(SO4)3,X为FeSO4,E为Fe,Z和KOH、Cl2反应生成K2EO4,Z为Fe(OH)3,再结合题目分析解答.
解答 解:(1)根据以上分析,M、E的化学式分别为Cu、Fe,故答案为:Cu;Fe;
(2)Cu、双氧水和稀硫酸发生氧化还原反应生成硫酸铜和水,反应方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,若参加反应H2O2为1mol,转移电子为2mol,故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;2;
(3)X中含有亚铁离子,亚铁离子能被氧气氧化生成铁离子,离子反应方程式为4Fe2++O2+4H+═4Fe3++2H2O,加入KI-淀粉溶液,溶液变为蓝色,说明碘离子被氧化生成碘单质,同时铁离子被还原生成亚铁离子,离子方程式为2Fe3++2I-=2Fe2++I2,
故答案为:4Fe2++O2+4H+═4Fe3++2H2O;2Fe3++2I-=2Fe2++I2;
(4)氯气和KOH、氢氧化铁反应生成高铁酸钾、氯化钾和水,反应方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O,故答案为:10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O.
点评 本题考查无机物推断,为高频考点,侧重考查学生分析推断能力,以某些物质颜色、离子特征反应为突破口采用正逆结合的方法进行推断,注意铁离子、双氧水的性质,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | c(H+) | B. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | C. | c(H+)•c(OH-) | D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3是10电子微粒 | |
| B. | 氨气易液化,液氨可用作制冷剂 | |
| C. | 蘸有浓盐酸的玻璃棒遇氨气产生的白烟 | |
| D. | 氨气是电解质,NH3•H2O是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质:胆矾、一水合氨、硫酸钡、CaO | |
| B. | 酸性氧化物:CO2、SO2、NO2、SiO2 | |
| C. | 混合物:铝热剂、干冰、水玻璃、盐酸 | |
| D. | 弱酸:氢碘酸、醋酸、碳酸、次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 300 mL0.1 mol/L NaCl溶液 | |
| B. | 100 mL0.1 mol/LFeCl3溶液 | |
| C. | 标准状况下,4.48LHC1气体溶于水配成的1 L溶液 | |
| D. | 向1 L0.2 mol/L BaCl2溶液中加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液(忽略溶液混合时的体积变化) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 的名称是2,2,4,5-四甲基-3,3-二乙基己烷
的名称是2,2,4,5-四甲基-3,3-二乙基己烷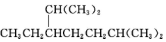 的名称为2,6-二甲基-3-乙基庚烷
的名称为2,6-二甲基-3-乙基庚烷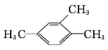 的名称是1,2,4-三甲苯
的名称是1,2,4-三甲苯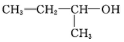 的名称是2-丁醇
的名称是2-丁醇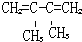 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
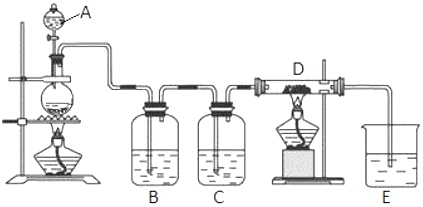
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
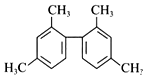
| A. | 分子中至少有11个碳原子处于同一平面上 | |
| B. | 分子中至少有10碳原子处于同一平面上 | |
| C. | 该烃核磁共振氢谱图中有4个吸收峰 | |
| D. | 该烃属于苯的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com