
| ||
| A、在Cu2O、Cu2S中Cu元素化合价都是+1价 |
| B、反应中Cu元素被氧化,S元素被还原 |
| C、Cu2S在反应中既是氧化剂,又是还原剂 |
| D、每生成6.4gCu,反应中转移0.1mol电子 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Fe3O4,反应转移的电子总数为2 mol | ||
| B、也可在酸性条件下用该方法制备Fe3O4纳米颗粒 | ||
C、反应每消耗1mol Fe2+,被Fe2+还原的O2的物质的量为
| ||
| D、x=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Na、Mg、Al的物质的量x | x<
|
| ③ | ④ | ||||
| 产生H2的体积 | ① | ② | V(Na)>V(Mg)=V(Al) | V(Na)=V(Mg)=V(Al) |
查看答案和解析>>
科目:高中化学 来源: 题型:
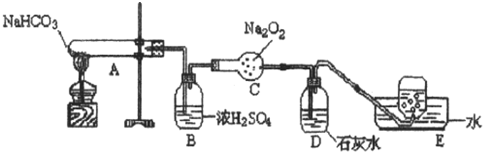
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K2MnO4 |
| B、MnSO4 |
| C、Mn2O3 |
| D、MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳离子不一定是金属离子,含阳离子的物质一定含阴离子 |
| B、阴、阳离子相互作用不一定形成离子化合物 |
| C、离子化合物均属于强电解质,都易溶于水 |
| D、由某金属元素的阳离子和某非金属元素阴离子组成的物质一定是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com