
【题目】化学反应速率与限度与生产、生活密切相关
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 688 | 810 | 860 |
①反应速率最大的时间段是(填0~1、1~2、2~3、3~4、4~5 )_____ min,原因是_____________。
②在2~3min时间段以盐酸的浓度变化来表示的反应速率为_________。(设溶液体积不变)
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列___________以减慢反应速率。(填写代号)
A.冰块 B.HNO3溶液 C.CuSO4溶液
(3)某温度下在10L密闭容器中,3种气态物质,A、B、C的物质的量随时间变化曲线如图。

①该反应的化学方程式是___________
②在该条件达到反应的限度(平衡状态)时反应物的转化率为____________
(转化率=(转化的物质的量/初始物质的量)×100%)(计算结果保留1位小数)
【答案】2~3 因该反应放热,随着反应,溶液温度升高,故反应速率加快 0.2 mol·L-1·min-1 A 2C ![]() A +3B 66.7%
A +3B 66.7%
【解析】
(1)①根据影响化学反应速率的因素有浓度、温度以及固体的表面积大小等因素分析,温度越高、浓度越大、固体表面积越大,反应的速率越大,从表中数据看出2 min~3 min收集的氢气比其他时间段多,原因是Zn置换H2的反应是放热反应,温度升高;
②根据v=△c/△t计算2~3分钟时间段以盐酸的浓度变化来表示的该反应速率;
(2)根据根据影响化学反应速率的因素以及氢气的量取决于H+的物质的量分析;
(3)①根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
②转化率=转化的物质的量/初始物质的量×100%,进行计算求解.
:(1)①从表中数据看出2 min~3 min收集的氢气比其他时间段多,虽然反应中c(H+)下降,但主要原因是Zn置换H2的反应是放热反应,温度升高,
答案:2~3;因该反应放热,随着反应,溶液温度升高,故反应速率加快;
②在2~3min时间段内,生成标况下氢气的体积为:688mL-240mL=448mL,n(H2)=0.02mol,由2HCl~H2可知:消耗盐酸的物质的量为0.04mol,
则υ(HCl)=△c/△t=0.04mol/(0.2L×1min)= 0.2 mol·L-1·min-1
答案:0.2 mol·L-1·min-1
(2)A.加入冰块后温度降低,反应速率减小,H+的物质的量不变,生成氢气的量也不变,满足条件,故A正确;
B.加入HNO3溶液,硝酸具有强氧化性,与金属反应生成NO,不会生成氢气,故B错误;
C.加入CuSO4溶液,锌与铜离子反应生成铜,构成铜锌原电池,加快了反应速率,故C错误;
答案:A
(3)①由图象可以看出,反应中A、B的物质的量增加,C的物质的量减少,则A、B为生成物,C为反应物,且△n(A):△n(B):△n(C)=1mol:3mol:2mol=1:3:2,则反应的化学方程式为:2C ![]() A +3B ;
A +3B ;
答案:2C ![]() A +3B;
A +3B;
②C为反应物,其初始物质的量为3mol,平衡时为1mol,则C的转化率为:![]() ×100%=66.7%;
×100%=66.7%;
答案:66.7%


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是

A. 原子半径:W>Z>Y>X
B. 气态氢化物的稳定性:W<Z<X<Y
C. Z的最高价氧化物的水化物可能为强碱
D. W的最高正化合价与负化合价的绝对值可能相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)科学家最近研制出利用太阳能产生激光,使海水分解。
①太阳光分解海水时,光能转化为_____能,水分解时,断裂的化学键是_____(填“离子键”或“共价键”)
②已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则2H2(g)+O2(g)=2H2O(l) H=_____kJ·mol-1
(2)美国NASA曾开发一种铁·空气电池,其原理如图所示,电池反应为2Fe+O2+2H2O=2Fe(OH)2,
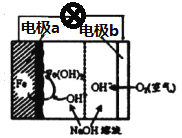
①Fe为原电池的______(填“正极”或“负极”),电极b上发生_____反应(填“氧化”或“还原”)。
②原电池工作一段时间后,若消耗铁22.4g,则电路中通过的电子数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为比较酸性条件下ClO—、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略)。
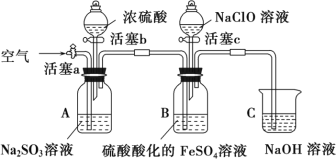
实验步骤及现象记录如下:
Ⅰ.打开活塞c,向装置B滴加次氯酸钠溶液,溶液立即变为黄色,一段时间后观察到装置B中液面上方出现黄绿色气体时,立即关闭活塞 c。
Ⅱ.用注射器取出少量装置B中的溶液,滴加几滴KSCN溶液,溶液变为血红色。
Ⅲ.打开活塞b,向装置A中加入足量浓硫酸后,关闭活塞b,装置A中产生气体,装置B中有气泡,一段时间后,观察到装置B中溶液黄色变浅绿色。
Ⅳ.一段时间后,用注射器取出少量装置 B 中的上层清液。
Ⅴ.打开旋塞a,通一段时间空气。
请回答下列问题:
(1)在添加药品前需进行的操作是__________________________。
(2)步骤Ⅰ中,一段时间后观察到装置B中液面上方出现黄绿色气体的离子方程式为____________。
(3)步骤Ⅲ中,开始一段时间,装置B中溶液的颜色并无明显变化,此段时间,溶液中发生反应的离子方程式为____________。
(4)步骤Ⅳ是为了验证该溶液中存在的Fe2+。请补充完整该步骤合理的操作及实验现象:_______。
(5)步骤Ⅴ的目的为______________。
(6)分析实验现象,可得出该实验的结论是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol·L1的FeCl2溶液中:H+、Al3+、SO42—、ClO
B. 无色透明的溶液中:Al3+、Fe3+、NO3—、SCN—
C. 与Al反应能放H2的溶液中:Cu2+、NH4+、CO32-、Cl
D. c(OH)/c(H+)=1×1014的溶液中:K+、Na+、I、SiO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g) ΔH。起始时只充入CH4与H2O(g),设
CO(g)+3H2(g) ΔH。起始时只充入CH4与H2O(g),设![]() =Z,保持反应压强不变,平衡时CH4的体积分数ω(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是
=Z,保持反应压强不变,平衡时CH4的体积分数ω(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是
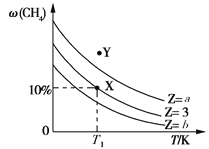
A. a>3>b
B. 保持温度不变,平衡体系加压后ω(CH4)增大
C. 温度为T1、Z=3时,Y点所对应的反应向逆反应方向进行
D. X点时,H2的体积分数为30%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉、铜粉加入到盛有FeCl3、FeCl2、CuCl2的混合液的烧杯中,判断下列情况烧杯中的固体及金属阳离子(用化学式表示):
(1)若反应后铁粉有剩余,则一定有______________。
(2)若反应后有Cu2+和Cu,则不可能有_________。
(3)若反应后有Cu2+和Fe3+,则一定有_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com