
【题目】下列有机物分子中,在氢核磁共振谱中信号强度(个数比)是1:3的是( )
A.邻二甲苯B.1,3,5-三甲基苯C.异丙醇D.对二甲苯
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】下列应用不涉及氧化还原反应的是
A.Na2O2用作呼吸面具的供氧剂 B.工业上电解熔融状态Al2O3制备Al
C.工业上利用合成氨实现人工固氮 D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:①2Sb2S3+3O2+6Fe![]() Sb4O6+6FeS;②Sb4O6+6C
Sb4O6+6FeS;②Sb4O6+6C![]() 4Sb+6CO↑;下列说法正确的是
4Sb+6CO↑;下列说法正确的是
A.反应②说明高温下Sb还原性比C强
B.反应①②中氧化剂分别是Sb2S3、Sb4O6
C.每生成1 mol Sb时,反应①与反应②中还原剂的物质的量之比为4︰3
D.反应①中每生成1 mol FeS时,共转移2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL FeI2溶液中逐渐通入Cl2,会依次生成I2、Fe3+、![]() ,其中Fe3+、I2的物质的量随通入Cl2的物质的量n(Cl2)的变化如图所示,下列说法不正确的是
,其中Fe3+、I2的物质的量随通入Cl2的物质的量n(Cl2)的变化如图所示,下列说法不正确的是

A.氧化性强弱:I2<Fe3+<![]()
B.n(Cl2)=0.12 mol时,溶液中的离子主要有:Fe2+、Fe3+、Cl
C.若n(Cl2)∶n(FeI2)=6∶5,反应的离子方程式为2Fe2++10I+6Cl2![]() 5I2+2Fe3++12Cl
5I2+2Fe3++12Cl
D.若n(Cl2)∶n(FeI2)=2∶1,反应的离子方程式为2Fe2++4I+3Cl2![]() 2I2+2Fe3++6Cl
2I2+2Fe3++6Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:C(s) + H2O(g)= CO(g) + H2(g),下列条件的改变对反应速率几乎无影响的是( )
A.增加CO的量B.保持体积不变,充入N2,使体系的压强增大
C.将容器的体积缩小一半D.保持压强不变,充入N2,使容器的体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护水资源刻不容缓。下列属于物理方法处理废水的是( )
A. 用生石灰处理酸性废水
B. 用沉淀剂处理含重金属离子的废水
C. 用稀盐酸处理碱性废水
D. 用沉降法处理废水中的固体颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用 0.10 mol·L-1的氨水滴定10.0mL a mol L-1的盐酸,溶液的pH与氨水体积(V)的关系如图所示。已知:N点溶液中存在:c(Cl-)=c(NH4+)+c(NH3·H2O)。下列说法不正确的是
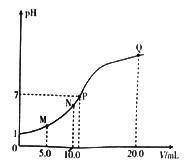
A. a=0.10
B. N、P两点溶液中水的电离程度:N
C. M、N两点溶液中NH4+的物质的量之比大于1:2
D. Q 点溶液中存在:2c(OH-)-2c(H+)=c(NH4+)-c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将13.6 g带铁锈的铁片溶解于25 mL、14 mol/L的热的浓硫酸中,气体只有SO2且体积为1.12 L(标准状况)。将溶液稀释至100 mL,所得溶液遇KSCN溶液时无血红色出现。下列结论正确的是
A.反应中:转移电子3.01×1022个 B.反应后:剩余硫酸0.30 mol
C.原混合物:n(Fe2O3)∶n(Fe)=1∶2 D.所得溶液:c(FeSO4)=1.7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的叙述错误的是
A.过滤操作中,漏斗的尖端应接触烧杯内壁
B.向容量瓶中转移液体时,引流用的玻璃棒可以接触容量瓶内壁
C.配制5%NaCl溶液时,必须用到的玻璃仪器是容量瓶、烧杯、胶头滴管、玻璃棒
D.分液漏斗、容量瓶及滴定管使用前都必须检漏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com