
| 乙 | 丙 | 丁 | |
| 甲 | 戊 |
分析 短周期元素甲、乙、丙、丁、戊在元素周期表中的位置,可知乙、丙、丁处于第二周期,甲、戊处于第三周期,丁所处的主族序数是其周期序数的三倍,最外层电子数为6,故丁为O,则乙为C、丙为N、甲为Si、戊为Cl,据此解答.
解答 解:根据短周期元素甲、乙、丙、丁、戊在元素周期表中的位置,可知乙、丙、丁处于第二周期,甲、戊处于第三周期,丁所处的主族序数是其周期序数的三倍,最外层电子数为6,故丁为O,则乙为C、丙为N、甲为Si、戊为Cl,
(1)甲为Si元素,在元素周期表中的位置是第三周期ⅣA族,故答案为:第三周期ⅣA族;
(2)同周期自左而右原子半径减小,同主族自上而下增大,故原子半径:甲>丁,故答案为:>;
(3)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,元素的非金属性:甲<丙,故答案为:<.
点评 本题考查结构性质位置关系应用,难度不大,侧重对元素周期律与化学用语考查.


科目:高中化学 来源: 题型:填空题
 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能说明盐酸是强酸:2HCl+CaCO3═CaCl2+CO2↑+H2O | |
| B. | 能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| C. | 能说明NH3结合H+能力比H2O强:NH3+H3O+═NH4++H2O | |
| D. | 能说明CH3COOH是弱电解质:CH3COO-+H2O?CH3COOH+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
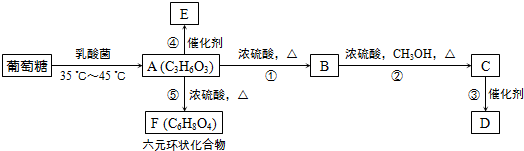
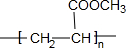 ,⑤2
,⑤2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是银白色的柔软金属(除铯外),密度都小于水 | |
| B. | 单质的熔、沸点随原子序数的增加而升高 | |
| C. | 原子半径随核电荷数的增大而增大 | |
| D. | 氧化能力最强的是铯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com