
【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
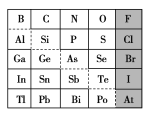
(1)元素Ga在元素周期表中的位置为:第________周期第________族。
(2)Sn的最高正价为________,Cl的最高价氧化物对应水化物的化学式为________,Bi的最高价氧化物为________。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________(填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________(填“>”“<”或“=”)H2S。
④原子半径比较:N________(填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)
【答案】4 ⅢA +4 HClO4 Bi2O5 F < < < CaCO3固体,盐酸,饱和NaHCO3溶液, Na2SiO3溶液
【解析】
根据各元素在周期表中的位置及元素周期律进行判断。
(1)B元素为第2周期第ⅢA族,和它同主族的相差两个电子层的是Ga元素,在第4周期第ⅢA族;
(2)碳、锡同为第IVA族,其最外层均有4个电子,所以Sn的最高价为+4;Cl最外层有7个电子,其最高价为+7价,最高价氧化物对应的水化物为HClO4;Bi的最外层有五个电子,其最高价氧化物为Bi2O5;
(3)①阴影部分为卤族元素。同主族元素从下往上,元素的非金属性逐渐增强,故卤族元素中F的非金属性最强,其对应的氢化物热稳定性最高;
②同周期元素,随着原子序数的递增,元素的非金属性越强,其最高价氧化物的水化物酸性也越强,所以H3AsO4酸性小于H2SeO4;
③氧的非金属性强于硫,所以H2O的还原性弱于H2S;
④由于原子半径Si>P,P>N,所以原子半径Si>N;
(4) 比较C、Si的非金属性强弱,可以通过比较H2CO3和H2SiO3的酸性强弱来实现,而比较两种酸的强弱可利用“复分解反应中强酸制弱酸的基本原理”。 选用稀盐酸与碳酸钙反应制取CO2,不选用稀硫酸与碳酸钙反应来生成二氧化碳,是因为会生成微溶的硫酸钙,覆盖在碳酸钙表面,阻止反应进一步进行。选用饱和NaHCO3溶液,以除去挥发出的HCl气体,不选用饱和Na2CO3,因为发生反应消耗了CO2:Na2CO3+CO2+H2O=2NaHCO3;将生成的CO2气体通过饱和碳酸氢钠溶液后再将气体通入Na2SiO3溶液。依据生成白色胶状沉淀,得出酸性H2CO3>H2SiO3,所以据此可判断出非金属性C>Si。本实验选择的试剂有:CaCO3固体,盐酸,饱和NaHCO3溶液, Na2SiO3溶液。


科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)由1H216O与2H217O所代表的物质中,共有__________种元素,_________种原子,16O、17O的关系为________。
(2)红热木炭放入浓硫酸产生气体过程的化学反应方程式______________________。
(3)硫酸型酸雨产生的原因________________________________(化学方程式)
(4)SO2通入酸性高锰酸钾溶液中的离子方程式____________________________
(5)现有2.96 g铁的硫化物在空气中完全反应,生成2.40 g红色粉末(Fe2O3),并放出有刺激性气味的气体。将该气体通入溴水中,溶液褪色。用离子方程式表示溴水褪色的原因:___________________;通过计算,该铁的硫化物化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某校化学研究性学习小组探究的过量的Fe与浓硫酸反应的实验:
I.甲同学设计如下实验验证反应得到的混合气体中含有SO2、H2、H2O
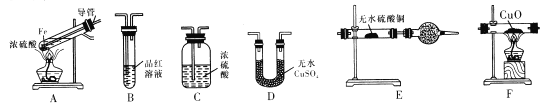
已知:CaSO3受热易分解
(1)写出过量Fe粉与浓硫酸反应产生等体积的SO2与H2的总化学方程式:________。
(2)若按气体从左到右的流向,为达到实验目的,各装置连接顺序是A→______(不可重复使用)。
(3)A中导管的作用为_____,装置E中的干燥管中盛放的物质为碱石灰,其作用是_______。
(4)证明有H2存在的实验现象是_________。
II.为测定混合气体中SO2的体积分数,,乙同学设计了如下实验方案:
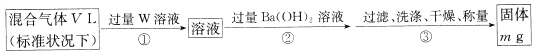
(5) W溶液可以是下列溶液中的______(填字母代号);
A.H2O2溶液 B.NaOH溶液 C.KMnO4溶液(硫酸酸化) D.氯水
该混合气体中二氧化硫的体积分数为_____________(用含V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求填空(化学方程式需注明反应条件):
(1) 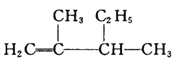 的系统名法名称是___________。
的系统名法名称是___________。
(2)反-2-丁烯的结构简式___________ 。
(3)分子式为C8H11N的有机物,含有苯环和—NH2结构的同分异构体有_________种。
(4)乙酸乙酯在酸性条件下水解的化学方程式____________ 。
(5)苯乙烯和1,3-丁二烯在一定条件下共聚合成丁苯橡胶的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合物的代数和为6;R和Q可形原子数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应.请回答下列问题:
(1)T元素在期表中的位置是________;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为________(写出其中一种物质的名称).
(2)X、Z、Q三种元素的原子半径由小到大顺序为________(填元素符号).
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为________.
(4)下列可以判断R和T金属性强弱的是________(填序号).
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为________;R2Q2与X2Q反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的电池,总反应为: 3Zn+2FeO42-+8H2O=2Fe(OH)3↓+3Zn(OH)2↓+4OH—,其工作原理如图所示。下列说法不正确的是
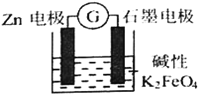
A. Zn极是负极,发生氧化反应
B. 随着反应的进行,溶液的pH增大
C. 电子由Zn极流出到石墨电极,再经过溶液回到Zn极,形成回路
D. 石墨电极上发生的反应为:FeO42—+3e—+4H2O=Fe(OH)3↓+5OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中烧杯里盛的是天然水,铁被腐蚀由快到慢的顺序是( )
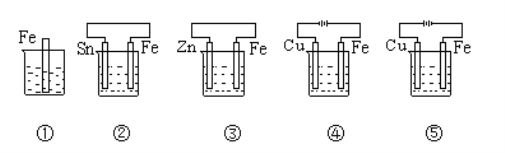
铁被腐蚀由快到慢的顺序是
A. ③〉②〉①〉④〉⑤ B. ④〉②〉①〉③〉⑤
C. ③〉②〉④〉⑤〉① D. ④〉⑤〉②〉③〉①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
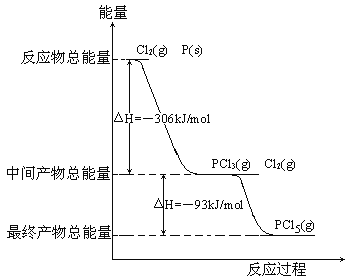
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式_________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________________________,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1等于_________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2_______α1(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是________________________________________。
(4)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com