
����Ŀ����ʵ�����������ͼ��ʾװ������ȡ�����ơ��������ƺ�̽����ˮ�����ʣ� ͼ�У�
��Ϊ��������װ�ã�
�ڵ��Թ���ʢ��15mL30%NaOH��Һ����ȡ�����ƣ���������ˮԡ�У�
�۵��Թ���ʢ��15mL8%NaOH��Һ����ȡ�������ƣ������ڱ�ˮԡ�У�
�ܵ��Թ��������ɫʯ����Һ��
��Ϊβ������װ�ã�
����д���пհף�
��1����ȡ����ʱ������ƿ�����һ�����Ķ������̣�ͨ�����������ƣ�����ƿ�м���������Ũ���ᣮʵ������Cl2�Ļ�ѧ����ʽΪ�� ʵ��ʱΪ�˳�ȥ�����е�HCl���壬���ڢ����֮�䰲װʢ������д���б����ĸ���ľ���װ�ã�
A����ʯ�� B������������Һ C������ʳ��ˮ D��Ũ����
��2���������������������20mL12molL��1��Ũ�����ϼ��ȣ���ַ�Ӧ�����ɵ�����0.06mol��������ڡ���С�ڡ����ڡ���������17.4g��MnO2����ԭ����������HCl�����ʵ���Ϊ ��
��3��д��װ�â��з�����Ӧ�Ļ�ѧ����ʽ ��
��4��ʵ���пɹ۲쵽�ܵ��Թ�����Һ����ɫ���������±仯������д�±��еĿհף�
ʵ������ | ԭ�� |
��Һ�������ɫ��Ϊ��ɫ | ������ˮ��Ӧ���ɵ�H+ʹʯ���ɫ |
�����Һ��Ϊ��ɫ | |
Ȼ����Һ����ɫ��Ϊɫ |
���𰸡�
��1����Һ©����MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O��C
MnCl2+Cl2��+2H2O��C
��2��С�ڣ�0.4mol
��3��3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
��4��HClO��ǿ�����ԣ�����Ư������������ɫ��dz�̣���Һ���ܽ��˴���������������dz��ɫ
���������⣺��1��ʵ�����Ʊ�������Ũ����Ͷ��������ڼ���������Ӧ��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O�����÷�Ӧ����Ϊ��Һ©����Բ����ƿ��������������HCl���壬�������������ڱ����Ȼ�����Һ��HCl������ˮ�����ñ���ʳ��ˮ���ӣ� �ʴ�Ϊ����Һ©����MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O�����÷�Ӧ����Ϊ��Һ©����Բ����ƿ��������������HCl���壬�������������ڱ����Ȼ�����Һ��HCl������ˮ�����ñ���ʳ��ˮ���ӣ� �ʴ�Ϊ����Һ©����MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O��C����2��������лӷ��ԣ����ȴٽ��Ȼ���Ļӷ������ŷ�Ӧ�Ľ��У������Ũ����С����������ֻ����Ũ���ᷢ����Ӧ����ϡ�����Ӧ�����Է�Ӧ�������������ʵ���С��0.06mol��17.4gMnO2�����ʵ���=
MnCl2+Cl2��+2H2O��C����2��������лӷ��ԣ����ȴٽ��Ȼ���Ļӷ������ŷ�Ӧ�Ľ��У������Ũ����С����������ֻ����Ũ���ᷢ����Ӧ����ϡ�����Ӧ�����Է�Ӧ�������������ʵ���С��0.06mol��17.4gMnO2�����ʵ���= ![]() =0.2mol���÷�Ӧ�ж������̺ͱ�������HCl�����ʵ���֮��Ϊ1��2����0.2mol�������̲μӷ�Ӧ������0.4molHCl��������
=0.2mol���÷�Ӧ�ж������̺ͱ�������HCl�����ʵ���֮��Ϊ1��2����0.2mol�������̲μӷ�Ӧ������0.4molHCl��������
�ʴ�Ϊ��С�ڣ�0.4mol����3������������Ϣ��֪���ڼ��������£�������ŨNaOH��Һ��Ӧ���������ơ��Ȼ��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O��
5NaCl+NaClO3+3H2O��
�ʴ�Ϊ��3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O����4��������ˮ��Ӧ��������ʹ����ᣬ��Ӧ���ɵ�H+ʹʯ���ɺ�ɫ�����������ǿ�����ԣ���ʯ������Ϊ��ɫ���ʣ����Է�Ӧ����Ϊ�ȱ�죬����ɫ����Ӧ�������ͨ����������������ˮ����Ϊ��������Һ����Һ�ʻ���ɫ��
5NaCl+NaClO3+3H2O����4��������ˮ��Ӧ��������ʹ����ᣬ��Ӧ���ɵ�H+ʹʯ���ɺ�ɫ�����������ǿ�����ԣ���ʯ������Ϊ��ɫ���ʣ����Է�Ӧ����Ϊ�ȱ�죬����ɫ����Ӧ�������ͨ����������������ˮ����Ϊ��������Һ����Һ�ʻ���ɫ��
�ʴ�Ϊ��
HClO��ǿ�����ԣ�����Ư������������ɫ | |
dz�� | ��Һ���ܽ��˴���������������dz��ɫ |
��1��ʵ�����Ʊ�������Ũ����Ͷ��������ڼ���������Ӧ�����÷�Ӧ����Ϊ��Һ©����Բ����ƿ�����ñ���ʳ��ˮ���ӣ���2���Ȼ����ӷ�����������ֻ����Ũ���ᷢ����Ӧ����ϡ�����Ӧ�����ݶ������̺�����ԭ����HCl֮��Ĺ�ϵʽ���㣻��3���ڼ��������£�������ŨNaOH��Һ��Ӧ���������ơ��Ȼ��ƺ�ˮ����4��������ˮ��Ӧ��������ʹ����ᣬ��Ӧ���ɵ�H+ʹʯ���ɺ�ɫ�����������ǿ�����ԣ���ʯ������Ϊ��ɫ���ʣ����Է�Ӧ����Ϊ�ȱ�죬����ɫ����Ӧ�������ͨ����������������ˮ����Ϊ��������Һ����Һ�ʻ���ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2O2�����NaHCO3��Ϲ������ܱ������г�ּ��ȷ�Ӧ���ų����������ʣ������ǣ� ��
A.NaOH��Na2O2B.NaOH��Na2CO3
C.Na2CO3D.Na2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵���У���ȷ����(����)
A.�����Ƶ�Cu(OH)2����Һ�ɼ�����Һ�е�������
B.�����Ҵ�����ϩ���ܷ����ӳɷ�Ӧ
C.ʯ�ͷ���ɻ����ϩ��������������
D.(NH4)2SO4��CuSO4����ʹ�����ʱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��°���ͼ��װ��ʵ��װ�ã�����ƿ��ʢ6.5 gп��(������С������ͬ)��ͨ����Һ©������40 mL 2.5 mol��L��1��������Һ����������H2�ռ���һ��ע�����У���ʱ10 sʱǡ���ռ�����������Ϊ50 mL(���ۺϳ�0 ����101 kPa�����µ�H2���Ϊ44.8 mL)���ڸ��¶��£�����˵������ȷ����(����)

A. ����ͨ���ⶨп�������������ⶨ��Ӧ����
B. ������ƿ����Һ����ı仯����H������ʾ10 s�ڸ÷�Ӧ������Ϊ0.01 mol��L��1��s��1
C. ������ƿ����Һ����ı仯����Zn2������ʾ10 s�ڸ÷�Ӧ����Ϊ0.01 mol��L��1��s��1
D. ��H2����ʾ10 s�ڸ÷�Ӧ������Ϊ0. 000 2 mol��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������;�㷺������������Ҫ�ɷ�ΪAl2O3nH2O������SiO2��Fe2O3����ȡAl������;���� 
��1����ҺA�ӹ���NaOH���ӷ���ʽ��ʾΪ
��2������ʱʢ��ҩƷ������������ ��
��3��������з�����Ӧ�Ļ�ѧ����ʽ�� ��
��4������������ɹ���C�����ӷ�Ӧ����ʽΪ ��
��5��ȡ��ҺB 100mL������1molL��1����200mL���������ﵽ���������Ϊ11.7g������ҺB��c��AlO ![]() ��= �� c��Na+��6molL��1�����������=����������
��= �� c��Na+��6molL��1�����������=����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̬��A��̼Ԫ������Ԫ�ص�������Ϊ6�U1.������һ��������ˮ�������B��B��������֯�л����������ų��������ṩ����������������й����ʵ�ת����ϵ����ͼ��
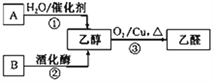
��ش�
��1���ٵķ�Ӧ������_________________��
��2�����Թ��м���2 mL10%����������Һ���μ�4��5��5%����ͭ��Һ�������2 mL10% B��Һ�����ȡ�д�����Ⱥ�۲쵽������_____________________________��
��3����Ӧ�۵Ļ�ѧ����ʽ��__________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����ʵ�鱨�����г������������к������� �� ��
A. �� 10mL��Ͳ��ȡ 5.12mL ϡ����
B. �ù㷺 pH ��ֽ���ij��Һ pH Ϊ 3.2
C. �� 25mL ��ʽ�ζ��ܣ���ȡij����Һ 20.50mL
D. ��������ƽ��ȡ 10.50 gNaCl ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������淴Ӧ2SO2(g)��O2(g)===2SO3(g)�ǹ�ҵ����ȡH2SO4����Ҫ��Ӧ��
��1���ں�ѹ�����£��÷�Ӧ����ʵ����й��������±���

��֪����������ʵ������У�SO3��������������(SO3)��ʱ��t�ı仯������ͼ��ʾ

������������Ȳ�ͬ��������________
�ڽ�����ʵ�����¶ȱ�Ϊ800 ��������(SO3)�ﵽa%����ʱ��________(����С������������������������)t1
��2�����ĸ������ͬ���ܱ������зֱ����һ������SO2��O2����ʼ��Ӧʱ������Ӧ�����ɴ�С����˳����ȷ����________
�ף���500 ��ʱ��10 mol SO2��10 mol O2��Ӧ
�ң���500 ��ʱ����V2O5��������10 mol SO2��10 mol O2��Ӧ
������450 ��ʱ��8 mol SO2��5 mol O2��Ӧ
������500 ��ʱ��8 mol SO2��5 mol O2��Ӧ
A.�ס��ҡ������� B���ҡ��ס������� C���ҡ��ס������� D�����������ҡ���
�� ������������Ի�ѧƽ���Ӱ��ش��������⣺
��1���ⵥ��������ˮȴ������KI��Һ����ˮ�м���KI��Һ������Ӧ��I2(aq)��I��(aq)![]() I3��(aq)������˵������ȷ����________(����ĸ��ţ���ͬ)��
I3��(aq)������˵������ȷ����________(����ĸ��ţ���ͬ)��
a��������ϵ�м��뱽��ƽ�ⲻ�ƶ�
b�������ø÷�Ӧԭ����ȥ����������ĵⵥ��
c��ʵ�������Ƶ�ˮʱ��Ϊ����ⵥ�ʵ��ܽ�ȿɼ�������KI��Һ
d������AgNO3��Һƽ�������ƶ�
��2��ij�¶��£����һ�����ܱ������н��з�Ӧ��N2(g)��3H2(g)![]() 2NH3(g)����H<0��
2NH3(g)����H<0��
�����з�����ȷ����________��
a��ƽ�����N2���÷�Ӧ����H����
b��ƽ�����������÷�Ӧ����H����
c��ƽ�����NH3����ƽ��ʱ��NH3�İٷֺ������
d������Ӧǰ�����N2��H2���ʵ�����ȣ���ƽ��ʱN2��ת���ʱ�H2�ĸ�
�������H2��ת���ʣ����д�ʩ���е���________��
a�����������
b���������а�ԭ�����ٳ���N2��H2
c�����������ٳ����������
d���ı䷴Ӧ�Ĵ���
e��Һ��NH3������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������У�̼����Ԫ�ص�������Ϊ��ֵ����
A.����B.������C.Ȳ��D.����ͬϵ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com