
| A. | 标准状况下,7.8g苯中含有的碳碳双键数是0.3NA | |
| B. | 标准状况下,11.2L四氯甲烷所含分子数为0.5NA | |
| C. | 常温常压下,14g乙烯分子中含有的碳碳键数目为2NA | |
| D. | 1mol氢氧根离子(OH-)所含电子数为10NA |
分析 A.苯分子中不存在碳碳双键;
B.标况下四氯化碳的状态不是气体;
C.根据n=$\frac{m}{M}$计算影响的物质的量,然后计算含有碳碳双键的数目;
D.氢氧根离子中含有10个电子,1mol氢氧根离子含有10mol电子.
解答 解:A.苯分子中的碳碳键为一种介于单键和双键之间的独特键,苯中不存在碳碳双键,故A错误;
B.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C.14g乙烯的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,0.5mol乙烯中含有0.5mol碳碳双键,含有的碳碳键数目为0.5NA,故C错误;
D.1mol氢氧根离子(OH-)含有10mol电子,所含电子数为10NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
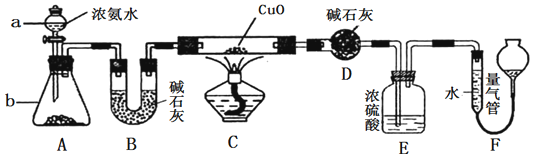
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
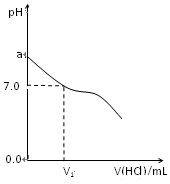 常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸.溶液的PH值的变化关系如图所示.
常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸.溶液的PH值的变化关系如图所示. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有两个电子的原子一定在IIA 族 | |
| B. | IA族均为碱金属 | |
| C. | 同一周期核电荷数越大原子半径越大 | |
| D. | 同一主族核电荷数越大元素金属性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气的性质很活泼,它与氢气混合后立即发生爆炸 | |
| B. | 可以用氢氧化钙溶液吸收实验室制取氯气时多余的氯气 | |
| C. | 检验Cl2中是否混有HCl方法是将气体通入硝酸银溶液 | |
| D. | 除去Cl2中的HCl气体,可将气体通入饱和食盐水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com