
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:
已知:FeS2和铁黄均难溶于水
下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS2+14Fe3++8H2O===15Fe2++2SO+16H+
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】乙烯是重要的有机原料,根据以下合成路线,回答问题。
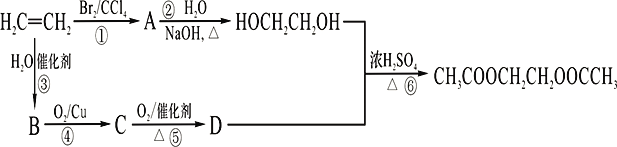
(1)写出乙烯的电子式_____________;A的名称为______________;
(2)B分子中的官能团名称是_________________;
(3)写出指定反应的反应类型:②________________,③______________;
(4)写出指定反应的化学方程式:④________________;⑥_____________。
(5)与B和D反应的生成物互为同分异构体,其中能和氢氧化钠反应的物质的结构简式_____________;
(6)HOCH2CH2OH能被酸性高锰酸钾氧化成E,写出E和HOCH2CH2OH生成高聚物的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中所含离子的浓度如下表,则M离子可能为( )
所含离子 | Cl﹣ | SO42﹣ | H+ | M |
浓度/(molL﹣1) | 2 | 1 | 2 | 1 |
A.Na+
B.Ba2+
C.NO3﹣
D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于ΔH(焓变)的说法正确的是( )
A. 在恒压件下,化学反应的焓变等于化学反应的反应热
B. ΔH>0时,反应放出热量;ΔH<0时,反应吸收热量
C. 需要加热才能发生的反应一定是吸热反应
D. 任何放热反应在常温下一定能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的说法正确的是( )
A.Mg和Al都可以用电解法冶炼得到
B.Mg和Fe在一定条件下与水反应都生成H2 和对应的碱
C.Fe和Cu常温下放入浓硝酸中发生的现象相同
D.Na2O和Na2O2与CO2反应产物也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g) + 3Y(g) ![]() 2Z(g),有关下列图像的说法不正确的是
2Z(g),有关下列图像的说法不正确的是
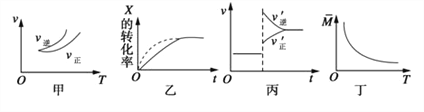
A. 依据图甲可判断正反应为放热反应
B. 在图乙中,虚线可表示使用了催化剂
C. 若正反应的ΔH<0,图丙可表示升高温度使平衡向逆反应方向移动
D. 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是________,还原剂是________,每生成1 mol Na2FeO4转移________mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用。________________________________
________________________________________________________________________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO![]() 、Cl-、H2O。
、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:___________________________。
②每生成1 mol FeO![]() 转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A元素的阴离子、B元素的阴离子和C元素的阳离子具有相同的电子层结构。已知A的原子序数大于B的原子序数。则根据元素周期律可知:A、B、C三种原子半径大小的顺序是( )
A. A > B > C B. B > A > C C. C > A > B D. C > B > A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com