
����Ŀ�������仯�����ת���Թ�ũҵ������������������Ҫ�����塣
��1�������ǵ����������ڼ��ֲ�ͬ����µ�ת����
����֪��2SO2(g)��O2(g)![]() 2SO3(g) ��H����196.6kJ��mol��1
2SO3(g) ��H����196.6kJ��mol��1
2NO(g)��O2(g)![]() 2NO2(g) ��H����113.0kJ��mol��1
2NO2(g) ��H����113.0kJ��mol��1
��SO2������NO2���巴Ӧ����SO3�����NO������Ȼ�ѧ����ʽΪ___��
��a.����Ⱥ����ܱ�������ͨ��SO2��NO2��һ��������ʹ�䷴Ӧ�ﵽƽ�⣬����Ӧ������ʱ��仯��ʾ��ͼ��ͼ1��ʾ����Ӧ��c��___(�����ﵽ������δ����)ƽ��״̬��
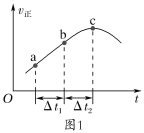
b.��ʼʱ���ֱ��ڸ������м����2molSO2(g)��2molNO2(g)����2molSO3(g)��2molNO(g)����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������__(����>������������<��)��
��2������ʱ��Ũ��Ϊ0.1mol��L-1���ΪV L�İ�ˮ����μ���һ��Ũ�ȵ����ᣬ��pH�Ʋ����Һ��pH����������ı仯������ͼ2��ʾ��d�㴦������Һǡ����ȫ��Ӧ������ͼ2�ش��������⣺
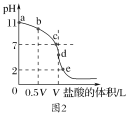
��b��c��d�����Ӧ����Һ�У�ˮ�����c(OH��)�ɴ�С��˳��Ϊ____��
�ڵζ�ʱ����b�㵽c��Ĺ����У����и�ѡ������ֵ���ֲ������___��
a.![]() b.
b.![]()
c.![]() d.
d.![]()
�۸��¶�ʱ��ˮ�ĵ���ƽ�ⳣ��K��___��
��3����������������Ⱦ��������������������Һ���ա������ķ�ӦΪ��
2NaOH��NO��NO2=2NaNO2��H2O
2NaOH��2NO2=NaNO3��NaNO2��H2O
����Ӧ���Һ������������Һ�ֱ�ӵ���ͼ3��ʾ�ĵ����н��е�⣬A�Ҳ���N2��
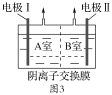
�ٵ缫����__����B�Ҳ�����������___��
��A��NO2-�����ĵ缫��Ӧ��__��
���𰸡�SO2(g)��NO2(g)![]() NO(g)��SO3(g)����H����41.8 kJ��mol��1 δ�� < d>c>b cd 10��5(��10��5 mol��L��1) �� O2 2NO2-��6e����4H2O=8OH����N2��
NO(g)��SO3(g)����H����41.8 kJ��mol��1 � < d>c>b cd 10��5(��10��5 mol��L��1) �� O2 2NO2-��6e����4H2O=8OH����N2��
��������
���������֪�����⿼���˹���ɡ���ѧƽ�ⳣ����������ʵĵ��롢���ԭ����֪ʶ�����ø�˹���ɡ���ѧƽ�ⳣ�����㹫ʽ��������ʵĵ�����ɡ����ԭ��������
(1) ����֪��a:2SO2(g)��O2(g)![]() 2SO3(g) ��H����196.6kJ��mol��1
2SO3(g) ��H����196.6kJ��mol��1
b:2NO(g)��O2(g)![]() 2NO2(g) ��H����113.0kJ��mol��1
2NO2(g) ��H����113.0kJ��mol��1
���ݸ�˹���ɣ���![]() ��, SO2 (g)+NO2(g)
��, SO2 (g)+NO2(g) ![]() NO(g)+SO3(g) ��H=-41.8 kJ��mol��1��
NO(g)+SO3(g) ��H=-41.8 kJ��mol��1��
�ʴ�Ϊ: SO2(g)��NO2(g)![]() NO(g)��SO3(g)����H����41.8 kJ��mol��1��
NO(g)��SO3(g)����H����41.8 kJ��mol��1��
��a.��Ӧ�ﵽƽ��ı�־��v��=v�����Ҳ��ٱ仯����c���Ӧ��v�����ڸı䣬�ʷ�Ӧ��c��δ��ƽ��״̬��
�ʴ�Ϊ: δ����
b.���������º��ݣ���ƽ�ⳣ������=��ʵ�����������ݾ���,SO2(g)+NO2(g) ![]()
NO(g)+SO3(g) ��H<0�����ڸ������м���2 molSO2(g) ��2molNO (g)��Ӧ�ų����������������м���2mol SO3(g)��2mol NO(g)����Ӧ�����������ݴ˷���ƽ�ⳣ������<��
�ʴ�Ϊ: <��
��2������b���Ӧ����Һ�У�����Ϊһˮ�ϰ����Ȼ�泥��Ҷ���Ũ����ȣ�����ͼ2��֪����Һ�ʼ��ԣ���һˮ�ϰ��ĵ���̶ȴ����Ȼ�淋�ˮ��̶ȣ���ʱˮ�ĵ����ܵ����ƣ���c���Ӧ����Һ�У�������Ϊһˮ�ϰ����Ȼ�泥�������Ũ�Ȳ���ȣ�����ͼ2֪��c����Һ�����ԣ����ʱһˮ�ϰ��ĵ���̶ȵ����Ȼ�淋�ˮ��̶ȣ�ˮ�ĵ��벻��Ӱ�죬��d���Ӧ����Һ�У�����Ϊ�Ȼ�泥��Ȼ�立���ˮ�⣬��Һ�����ԣ���ˮ�ĵ�����ٽ����ã�����b��c��d�����Ӧ����Һ�У�ˮ�����c��OH-����С˳��Ϊd>c>b��
�ʴ�Ϊ: d>c>b��
�ڵζ�ʱ����b�㵽c��Ĺ����У���Һ���Լ�����������ǿ��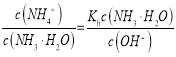 ����b�㵽c��Ĺ����У�c��OH-�����ϼ�С���ʸ�ֵ����a���������⣻
����b�㵽c��Ĺ����У�c��OH-�����ϼ�С���ʸ�ֵ����a���������⣻
��b�㵽c��Ĺ����У�c��H+����������c��OH-�����ϼ�С��![]() ��ֵ������b���������⣻
��ֵ������b���������⣻
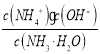 ��ֵ����һˮ�ϰ��ĵ���ƽ�ⳣ������Kb��NH3��H2O��ֻ���¶��йأ��ζ��������¶Ȳ��䣬��
��ֵ����һˮ�ϰ��ĵ���ƽ�ⳣ������Kb��NH3��H2O��ֻ���¶��йأ��ζ��������¶Ȳ��䣬��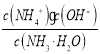 ��ֵ���䣬c�������⣻
��ֵ���䣬c�������⣻
 ��ֵ����笠����ӵ�ˮ��ƽ�ⳣ����b�㵽c������в��䣬d
��ֵ����笠����ӵ�ˮ��ƽ�ⳣ����b�㵽c������в��䣬d
�ʴ�Ϊ: cd��
��δ������ʱ����ˮŨ��Ϊ0.1mol/L����Һ��pH=11������Һ��![]() ��ˮ�ĵ���̶Ƚ�С����Һ��c(OH-)��c(NH4+)����һˮ�ϰ��ĵ���̶Ƚ�С����c(NH3��H2O)=0.1mol/L����ˮ�ĵ���ƽ�ⳣ��
��ˮ�ĵ���̶Ƚ�С����Һ��c(OH-)��c(NH4+)����һˮ�ϰ��ĵ���̶Ƚ�С����c(NH3��H2O)=0.1mol/L����ˮ�ĵ���ƽ�ⳣ��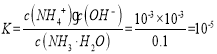 ��
��
�ʴ�Ϊ: 10��5(��10��5 mol��L��1)��
(3)��A�Ҳ���N2����֪A�ҵĵ������ҺΪNaNO3��NaNO2�Ļ����Һ��NO2-�ڵ缫���Ϸŵ�����N2���缫��ӦʽΪ2NO2-��6e����4H2O=8OH����N2������缫��Ϊ�������缫Ϊ��������B�ҵĵ������ҺΪNaOH��Һ��OH-�ڵ缫���Ϸŵ�����O2��
�ʴ�Ϊ: ���� O2�� 2NO2-��6e����4H2O=8OH����N2����


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ƶ�˵���в���ȷ����( )
A.�����ƺ�������Ӧ��������ͬ��������ͬ
B.�Ƴ��ڷ����ڿ����У����ս����̼����
C.�ƵĻ�ѧ���ʱȽϻ��ã��������ƿ��Ա�����ú����
D.�����Ż�ʱ����ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƽ����ϵmA(g)+nB(g)=C(g)+gD(g)����H<0�����н����д�����ǣ� ��
A.���¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������m+n<p+q
B.��m+n=p+q����������amol�����ƽ����ϵ���ټ���amol��B���ﵽ��ƽ��ʱ������������ʵ�������2a
C.���¶Ȳ��䣬ѹǿ����ԭ����2�����ﵽ��ƽ��ʱ�������һ����ԭ����![]() ҪС
ҪС
D.��ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͭƬ��![]() Ũ������ȳ�ַ�Ӧ���ռ�����״���µ�
Ũ������ȳ�ַ�Ӧ���ռ�����״���µ�![]() ����VL�����жԴ˷�Ӧ���й�˵���д������
����VL�����жԴ˷�Ӧ���й�˵���д������ ![]()
A. �÷�Ӧ������Ũ��������Ժ�ǿ������
B. ��Ӧ���������ַ�Ӧ�����ʣ��
C. ����ԭ������Ϊ![]()
D. �μӷ�Ӧ��CuΪ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�п��Է��������������ЧӦ�Ļ�ѧ���ʡ����������ᣬ��������Ľṹ��ʽ��ͼ��ʾ�������й�˵����ȷ���ǣ� ��
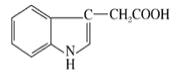
A.�����к���2�ֹ�������������
B.1mol������������������������Ӧ���������5molH2.
C.�������ᱽ���ϵĶ��ȴ��ﹲ������
D.�����к�һ������̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����������ơ�ͼ�Ρ���;��ʹ�ò�������������ȷ���ǣ� ��
ѡ�� | A | B | C | D |
���� | 250 mL����ƿ | ��Һ©�� | ��ʽ�ζ��� | ������ |
ͼ�� |
|
|
|
|
��;��ʹ�ò��� | ����1.0 mol��L��1NaCl��Һ������ʱ���ӿ̶ȣ�����õ���ҺŨ��С��1.0 mol��L��1 | �ø�����ȡ��ˮ�еĵ⣬��Һʱ���������Ͽڷų� | ��������ȡ10.00mL ������ˮ��Һ | ����ʵ���н���������ΪҺ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ģ��ϳɰ��Ͱ���������������ͼ��

��֪ʵ���ҿ��ñ�����������(NaNO2)��Һ�뱥���Ȼ����Һ�����Ⱥ�Ӧ��ȡ������
(1)��ͼ��ѡ����ȡ����ĺ���װ�ã�����___������___��
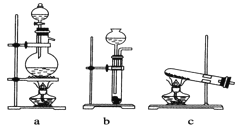
(2)����������ͨ����װ�ã���װ�õ����ó��˽��������⣬�����������ã��ֱ��ǣ�___��___��

(3)����װ������һ��ʱ�䰱����ͨ�������ͬʱ�������ȵIJ�˿������װ�õ���ƿ�ڣ���ʹ��˿���ֺ��ȵ�ԭ����___����ƿ�л��ɹ۲쵽��������___��
(4)д����װ���а������Ļ�ѧ����ʽ��___��
(5)��Ӧ��������ƿ�ڵ���Һ�г�����H+��OH-�⣬������___��___���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪XΪһ�ֳ������Ũ��Һ����ʹ���Ƿ�ĩ��ڣ�A��X��Ӧ��ת����ϵ��ͼ��ʾ�����з�Ӧ���������ֲ��������ȥ���������й�˵����ȷ����
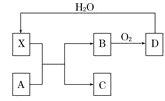
A. Xʹ���DZ�ڵ�������Ҫ������ X��ǿ������
B. ��AΪ������A��X�������²��ᷴӦ
C. ��AΪ̼���ʣ���Cͨ�������ijΜ[ʯ��ˮ�У���Һ��Ȼ����
D. ��ҵ���ڸ��¡���ѹ��ʹ�ô����������£�����ʹB��ȫת��ΪD
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3-��-1-�嶡���3-��-2-�嶡��ֱ���NaOH���Ҵ���Һ���ȣ���������Ӧ��˵����ȷ����( )
A.������ͬ����Ӧ������ͬB.���ﲻͬ����Ӧ������ͬ
C.̼������ѵ�λ����ͬD.̼������ѵ�λ����ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com