
【题目】恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g)![]() xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x=____________
(2)从反应开始到10s,B的平均反应速率为____________
(3)从反应开始到40s达平衡状态,A的平均反应速率为____________
(4)平衡时容器中B的体积分数为____________
(5)下列各项能表示该反应达到平衡状态是____________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量n(A)∶n(B)=2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
【答案】3 0.0075mol·L 1·s 1 0.01mol·L 1·s 1 40% CE
【解析】
⑴先计算A和C的改变量,再根据改变量之比等于计量系数之比建立关系。
⑵根据速率之比等于计量系数之比建立关系。
⑶计算B的改变量,根据改变量之比等于计量系数之比算A的改变量,再计算A的平均反应速率。
⑷根据⑶得到平衡时n(B),由于反应是等体积反应,根据体积分数计算。
⑸A.消耗A,正向反应,生成D,正向反应,同一个方向,不能说明达到平衡;B.容器中物质的物质的量之比不能说明达到平衡;C.气体的平均相对分子质量等于气体质量除以气体的物质的量,正向反应,气体质量减少,气体物质的量不变,气体的平均相对分子质量减少,当气体的平均相对分子质量不再变化说明达到平衡;D.反应是等体积反应,压强始终不变,因此压强不再变化不能说明达到平衡;E.气体密度等于气体质量除以容器体积,正向反应,气体质量减少,容器体积不变,气体密度减少,当气体密度不再变化说明达到平衡。
⑴10s时,测得A的物质的量为1.7mol,Δn(A)=2mol1.7mol =0.3mol,C的反应速率为0.0225mol·L 1·s 1;Δn(C)=υ(C)Vt=0.0225mol·L 1·s 1×2L×10s=0.45mol,根据改变量之比等于计量系数之比,得到0.3mol :0.45mol = 2:x,则x=3;故答案为:3。
⑵从反应开始到10s,根据速率之比等于计量系数之比,υ(C):υ(B)=3:1=0.0225mol·L 1·s 1:υ(B),解得υ(B)=0.0075 mol·L 1·s 1;故答案为:0.0075 mol·L 1·s 1。
⑶40s时反应恰好处于平衡状态,此时B的转化率为20%,Δn(B)= 2mol×20%=0.4mol,根据改变量之比等于计量系数之比,Δn(A):Δn(B) =Δn(A):0.4mol=2:1,Δn(A)= 0.8mol,从反应开始到40s达平衡状态,A的平均反应速率为![]() ;故答案为:0.01mol·L 1·s 1。
;故答案为:0.01mol·L 1·s 1。
⑷根据⑶得到平衡时n(B)=2mol0.4mol=1.6mol,由于反应是等体积反应,因此总气体物质的量为4mol,因此平衡时容器中B的体积分数为![]() ;故答案为:40%。
;故答案为:40%。
⑸A.消耗A,正向反应,生成D,正向反应,同一个方向,不能说明达到平衡,故A不符合题意;B.容器中物质的物质的量之比不能说明达到平衡,故B不符合题意;C.气体的平均相对分子质量等于气体质量除以气体的物质的量,正向反应,气体质量减少,气体物质的量不变,气体的平均相对分子质量减少,当气体的平均相对分子质量不再变化说明达到平衡,故C符合题意;D.反应是等体积反应,压强始终不变,因此压强不再变化不能说明达到平衡,故D不符合题意;E.气体密度等于气体质量除以容器体积,正向反应,气体质量减少,容器体积不变,气体密度减少,当气体密度不再变化说明达到平衡,故E符合题意;综上所述,答案为CE。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测被德国化学家合成证实。[18]-轮烯是一种大环轮烯,其结构简式如图所示。 有关它的说法正确的是

A.[18]- 轮烯分子中所有原子不可能处于同一平面
B.[18]- 轮烯的分子式为:C18H12
C.1 mol[18]- 轮烯最多可与9 mol氢气发生加成反应生成环烷烃
D.[18]- 轮烯与乙烯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+……,然后测定其质荷比。某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )
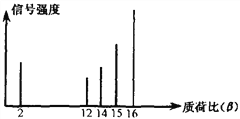

A. 甲醇 B. 丙烷 C. 甲烷 D. 乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】事物是相互影响、相互制约的。在有机化合物分子中,这种相互影响、相互制约同样存在。例如:
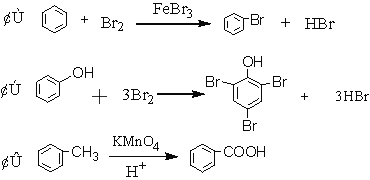
下列性质不能说明基团之间相互影响的是( )
A. ②用浓溴水而①用液溴;①需用催化剂而②不需用。
B. ②生成三溴取代产物而①只生成一溴取代产物。
C. CH3CH2OH无明显酸性,而![]() 显弱酸性。
显弱酸性。
D. 乙醇能使酸性高锰酸钾溶液褪色,而苯酚不能。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是

A.电极a为电解池阴极
B.阳极上有反应HSO3—-2e—+H2O=SO42—+3H+发生
C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2
D.处理后可得到较浓的H2SO4和NaHSO3产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A为淡黄色固体,B的阳离子与A相同(其他物质均略去).

根据以上关系,回答下列问题:
(1)A的电子式为__________.
(2)A投入FeCl2溶液中的反应为_______________(请用一个化学方程式表示)
(3)若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,则剩余的固体为_____________________________(写化学式)
(4)氢能被视为21世纪最具发展潜力的清洁能源,试回答下列问题:
①与化石燃料相比,氢气作为燃料的优点是__________________(答两点)。
②施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气,写出NaBH4与水反应的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子价电子排布图为______________(轨道表达式)。第四电离能I4(Co)比I4(Fe)小,是因为_____________________。
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是_________________________.
(3)乙炔(C2H2)分子中δ键与π键的数目之比为_______________。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___________;与该阴离子互为等电子体的分子有_____________。(列一种)
②碳酸亚乙酯分子中碳原子的杂化方式有_______________________。
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为______________。
②设NA为阿伏加德罗常数的值,Li2S的晶胞密度为____________(列出计算式)![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法一定正确的是( )

A.一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42-、Fe3+
B.一定存在H+、Al3+、NH4+、SO42-,可能存在Na+、Mg2+
C.溶液中c(H+):c(Al3+):c(Mg2+)=1:1:2
D.溶液中c(H+)/c(SO42-)![]() 2/9
2/9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA
B. 标准状况下,22.4L氖气含有的电子数为10NA
C. 常温下,![]() 的醋酸溶液中含有的
的醋酸溶液中含有的![]() 数为
数为![]()
D. 120g NaHSO4分子中阳离子和阴离子的总数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com