
【题目】某研究小组为探究影响过氧化氢分解的因素,做了三个实验。相应的实验结果如下图所示,请分析回答:
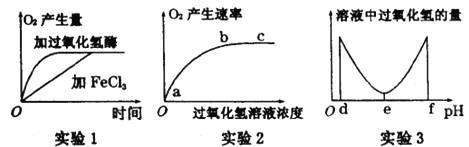
(1)实验1、2、3中的自变量分别为 。
(2)实验1的目的是探究 。
(3)实验2探究了过氧化氢溶液的浓度对过氧化氢酶的影响,该实验的结果显示 ,be段O2产生速率不再增大的原因最可能是 。
(4)实验3的结果显示,过氧化氢酶的最适pH为 。实验还证实,当pH小于d或大于f时,过氧化氢酶的活性将永久丧失,其原因是 。
【答案】(1)催化剂种类、过氧化氢的浓度、pH
(2)酶的高效性
(3)在过氧化氢酶量一定时,在一定浓度范围内,过氧化氢溶液浓度越高,O2产生速率越快,而当过氧化氢溶液浓度达到一定值后,02产生速率不再随过氧化氢浓度的增大而增大 过氧化氢酶的量有限
(4)e 过酸、过碱会导致酶的空间结构被破坏
【解析】(1)由曲线图分析可知,实验1,2,3中的自变量分别为催化剂的种类、H2O2浓度、pH。
(2)实验1用了无机催化剂和酶同时催化过氧化氢分解,此实验的目的是探究酶的高效性。
(3)实验2探究了过氧化氢溶液的浓度对过氧化氢酶的影响,该实验的结果显示在过氧化氢酶量一定时,在一定浓度范围内,过氧化氢溶液浓度越高,O2产生速率越快,而当过氧化氢溶液浓度达到一定值后,02产生速率不再随过氧化氢浓度的增大而增大。be段显示反应物的不断增加,不能影响O2产生速率,其氧气不再增大的原因最可能是催化剂过氧化氢酶的数量有限。
(4)实验3的结果显示,过氧化氢酶的最适pH为e,当pH小于d或大于f时,酶的空间结构被破坏,导致过氧化氢的活性将永久丧失。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列括号中的分离方法运用不得当的是( )
A. 碳酸钠和碳酸钙(过滤)
B. 水溶液中的食盐和碘(分液)
C. 碳酸钙和氯化钙(溶解 过滤 蒸发)
D. 自来水中的杂质(蒸馏)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KAl(SO4)212H2O(明矾)是一种复盐,在造纸等方面应用广泛.实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示.回答下列问题:![]()
(1)为尽量少引入杂质,试剂①应选用(填标号).
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为 .
(3)沉淀B的化学式为;将少量明矾溶于水,溶液呈弱酸性,其原因是 .
(4)已知:Kw=1.0×10﹣14 , Al(OH)3AlO2﹣+H++H2O K=2.0×10﹣13 . Al(OH)3溶于NaOH溶液反应的平衡常数等于 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于摩尔质量叙述中正确的是
A.1 mol CO的质量是28 g·mol1
B.硫酸根离子的摩尔质量是98 g
C.Cl2的摩尔质量是71 g·mol1
D.NaCl的相对分子质量是58.5 g·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A.1 mol任何物质都含有6.02×1023个原子
B.0.012 kg 12C约含有6.02×1023个碳原子
C.阿伏加德罗常数表示的粒子“集体”就是1 mol
D.使用摩尔这一单位时必须指明粒子的名称
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组研究镉、铜对河蚌过氧化氢酶活性的影响,用一定浓度的镉、铜处理河蚌一段时间后,测得河蚌过氧化氢酶活性如表所示.

请回答下列问题:
(1)表中a应是 。
(2)请列举本实验需要控制的无关变量: 。(至少写出两个)
(3)进行过氧化氢酶活性测定时,选过氧化氢为底物,用一定条件下单位时间的 来表示。
(4)若测定镉和铜对河蚌过氧化氢酶活性的综合影响作用,本实验应如何完善? 。
(5)能否用河蚌过氧化氢酶作为实验材料来探究温度对酶活性的影响?为什么? 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修3--物质结构与性质]M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题:
(1)单质M的晶体类型为 , 晶体中原子间通过作用形成面心立方密堆积,其中M原子的配位数为 .
(2)元素Y基态原子的核外电子排布式为 , 其同周期元素中,第一电离能最大的是(写元素符号).元素Y的含氧酸中,酸性最强的是(写化学式),该酸根离子的立体构型为 .
(3)M与Y形成的一种化合物的立方晶胞如图所示.
①该化合物的化学式为 , 已知晶胞参数a=0.542nm,此晶体的密度为gcm﹣3 . (写出计算式,不要求计算结果.阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是 . 此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列有关说法正确的是( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1mol氦气含有的原子数为2NA
C.71gCl2所含原子数为2NA
D.23g钠在化学反应中失去电子数目为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com