
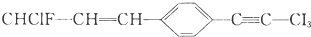
 关于该分子结构的说法正确的是( )
关于该分子结构的说法正确的是( )| A. | 除苯环外的其余碳原子有可能都在一条直线上 | |
| B. | 除苯环外的其余碳原子不可能都在一条直线上 | |
| C. | 12个碳原子不可能都在同一平面上 | |
| D. | 12个碳原子一定都在同一平面上 |
分析 根据 的结构可知,分子中含有碳碳双键,相当于乙烯的结构,碳碳参键,相当于乙炔的结构,另外苯环上所有原子都共面,处于对位的四个原子共线,
的结构可知,分子中含有碳碳双键,相当于乙烯的结构,碳碳参键,相当于乙炔的结构,另外苯环上所有原子都共面,处于对位的四个原子共线,
A.乙炔是直线型结构,乙烯是平面方形;
B.苯的同系物指含有1个苯环,侧链为烷基;
C.乙烯和苯是平面型结构,乙炔是直线型结构;
D.乙烯和苯是平面型结构,乙炔是直线型结构.
解答 解:根据 的结构可知,分子中含有碳碳双键,相当于乙烯的结构,碳碳参键,相当于乙炔的结构,另外苯环上所有原子都共面,处于对位的四个原子共线,
的结构可知,分子中含有碳碳双键,相当于乙烯的结构,碳碳参键,相当于乙炔的结构,另外苯环上所有原子都共面,处于对位的四个原子共线,
A.乙炔是直线型结构,乙烯是平面方形,则除苯环以外的其余碳原子不可能都在一条直线上,故A错误;
B.乙炔是直线型结构,乙烯是平面方形,则除苯环以外的其余碳原子不可能都在一条直线上,故B正确;
C.乙烯和苯是平面型结构,乙炔是直线型结构,12个碳原子可能都在同一平面上,故C错误;
D.乙烯和苯是平面型结构,乙炔是直线型结构,12个碳原子有可能都在同一平面上,但不一定,故D错误.
故选B.
点评 本题主要考查有机化合物的结构特点,难度不大,做题时注意从乙烯、苯和乙炔的结构特点判断有机分子的空间结构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
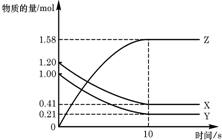 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
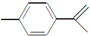 ,下列关于这种物质的说法中不正确的是( )
,下列关于这种物质的说法中不正确的是( )| A. | 该物质难溶于水 | |
| B. | 分子式为C10H14 | |
| C. | 既能发生取代反应,又能发生加成反应 | |
| D. | 既能使酸性高锰酸钾褪色又能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数是99 | B. | 质量数是43 | C. | 中子数是99 | D. | 电子数是43 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应时.增加水的用量 | |
| B. | Al与稀硫酸反应制取H2时.改用浓硫酸 | |
| C. | Na2SO4与BaCl2两种溶液反应时.增大压强 | |
| D. | 大理石和盐酸反应制取C02时.将块状大理石改为粉末状 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应③为N2O4═2NO2 | |
| B. | 该过程最终会导致大气中O的含量增加 | |
| C. | 总反应中NO2作催化剂 | |
| D. | 该反应可用于修复大气“臭氧空调” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com