
【题目】菠萝酯(Ⅰ)是一种具有菠萝香味的食用香料,其合成路线如图:
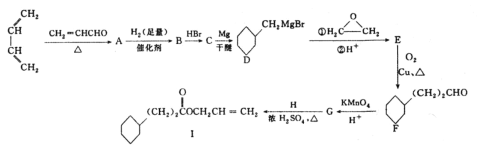
已知:ⅰ.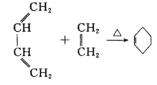
ⅱ.RMgBr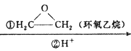 RCH3CH2OH+
RCH3CH2OH+
回答下列问题:
(1)A中所含官能团的名称是__,H的一种同分异构体能发生银镜反应,其化学名称是__(填化学名称)。
(2)G的结构简式是__,G到I的反应类型是__。
(3)E→F的化学方程式是__。
(4)I在一定条件下可合成高分子M,则M的结构简式是__。
(5)E在一定条件下发生消去反应得化合物N,N与CH2=CHCH=CH2在加热条件下反应产物的结构简式是__。
【答案】碳碳双键、醛基 丙醛  酯化反应(或取代反应) 2
酯化反应(或取代反应) 2 +O2
+O2![]() 2
2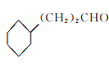 +2H2O
+2H2O 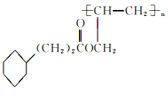

【解析】
![]() 与
与![]() 发生信息ⅰ的反应生成A(
发生信息ⅰ的反应生成A(![]() ),
),![]() 与足量氢气发生加成反应得到醇,醇和HBr发生取代反应得到C(
与足量氢气发生加成反应得到醇,醇和HBr发生取代反应得到C(![]() ),
),![]() 与Mg反应生成D,D与环氧乙烷发生信息ⅱ的反应生成E(
与Mg反应生成D,D与环氧乙烷发生信息ⅱ的反应生成E( ),
), 催化氧化反应生成F,F在酸性高锰酸钾的作用下氧化生成G(
催化氧化反应生成F,F在酸性高锰酸钾的作用下氧化生成G( ),G和CH2=CHCH2OH发生酯化反应得到I。
),G和CH2=CHCH2OH发生酯化反应得到I。
⑴根据信息ⅰ得到A中所含官能团的名称是碳碳双键、醛基,根据G和H反应生成I,得到H的结构简式为CH2=CHCH2OH,H的一种同分异构体能发生银镜反应,则结构简式为CH3CH2CHO,其化学名称是丙醛;故答案为:碳碳双键、醛基;丙醛。
⑵根据F与酸性高锰酸钾反应得到G的结构简式是 ,根据G、I的结构简式得到G到I的反应类型是酯化反应;故答案为:
,根据G、I的结构简式得到G到I的反应类型是酯化反应;故答案为: ;酯化反应(或取代反应)。
;酯化反应(或取代反应)。
⑶E→F是醇催化氧化变为醛,其化学方程式是2 +O2
+O2![]() 2
2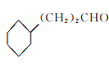 +2H2O;故答案为:2
+2H2O;故答案为:2 +O2
+O2![]() 2
2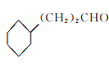 +2H2O。
+2H2O。
⑷I含有碳碳双键,发生加聚反应,在一定条件下可合成高分子M,则M的结构简式是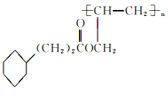 ;故答案为:
;故答案为: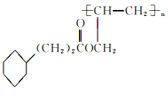 。
。
⑸E在一定条件下发生消去反应得化合物N(![]() ),N(
),N(![]() )与CH2=CHCH=CH2在加热条件下发生信息ⅰ反应,其反应产物的结构简式是
)与CH2=CHCH=CH2在加热条件下发生信息ⅰ反应,其反应产物的结构简式是 ;故答案为:
;故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础。下列关于各实验装置的叙述正确的是( )

A. 装置①常用于分离互不相溶的液体混合物
B. 装置②可用于吸收NH3或HCl气体,并防止倒吸
C. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
D. 装置③可用于收集H2、CO2、Cl2、NH3等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。在500℃下合成甲醇的反应原理为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
①反应进行到4 min 时,υ(正)__ (填“>”“<”或“=”)υ(逆)。0~4 min,H2的平均反应速率υ(H2)=__ mol·L-1·min-1。
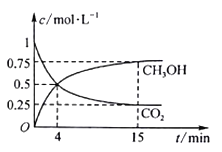
②CO2平衡时的体积分数为_____,该温度下Kp为_____(用含有p0的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是

A. 放电时,多孔碳材料电极为负极
B. 放电时,外电路电子由多孔碳材料电极流向锂电极
C. 充电时,电解质溶液中Li+向多孔碳材料区迁移
D. 充电时,电池总反应为Li2O2-x=2Li+(1-![]() )O2
)O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列结论错误的是 ( )

A. 完全电解2 mol H2O断裂的σ键键数为4NA
B. 标准状况下,11.2 L CO2中含有的π键键数为2NA
C. 60 g SiO2晶体中含有的Si—O键键数为4NA
D. 128 g金属铜中含有如图所示的晶胞数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具![]() 水热法制备Fe3O4纳米颗粒的反应是:3Fe2+ + 2S2O32-+ O2 + xOH- = Fe3O4↓+ S4O62- + 2H2O 。下列说法不正确的是
水热法制备Fe3O4纳米颗粒的反应是:3Fe2+ + 2S2O32-+ O2 + xOH- = Fe3O4↓+ S4O62- + 2H2O 。下列说法不正确的是![]()
![]()
A.参加反应的氧化剂与还原剂的物质的量之比为1:5
B.若有2molFe2+ 被氧化,则被Fe2+还原的O2的物质的量为0.5mol
C.每生成1molFe3O4,反应转移的电子为4mol
D.O2是氧化剂,S2O32-与Fe2+是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.0 L恒容密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)![]() Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 ( )
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 ( )

A. 该温度下此反应的平衡常数K=3.2
B. 从反应开始到t1时的平均反应速率v(X)=0.2/t1 mol·L-1·min-1
C. 欲提高平衡体系中Y的百分含量,可加入一定量的X
D. 其他条件不变,再充入0.1 mol气体X,平衡正向移动,X的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是前四周期元素,原子序数依次增大,根据表中提供的有关信息,回答问题:
元素 | 相关信息 |
A | 所有单质中密度最小 |
B | 形成化合物种类最多的元素 |
D | 基态原子中只有3个能级,有2个未成对电子 |
E | 短周期中原子半径最大 |
F | 第三周期中电负性最大的元素 |
G | 最外层只有一个电子,内层填满电子 |
(1)E元素在周期表中的位置是______,F元素原子最外层电子排布式为______,BD2的立体构型为______。
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:______。
(3)氢化物稳定性:B______D;最高价氧化物对应的水化物酸性:C______F。(填“<”或“>”)
(4)每个B2A4分子中含有______个σ键,______个π键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知伞形酮可用雷琐苯乙酮和苹果酸在一定条件下反应制得
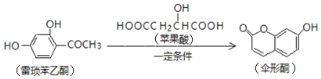
下列说法中正确的是( )
A.一分子反应物雷琐苯乙酮含有3个碳碳双键
B.苹果酸的一种缩聚产物是![]()
C.1mol产物伞形酮与足量NaOH溶液反应,最多可消耗2molNaOH
D.反应中涉及到的三种有机物都能跟FeCl3溶液发生显色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com