
【题目】现有短周期A、B、C、D四种元素,它们的原子序数依次增大,A元素形成的-2价阴离子比氦原子的核外电子数多8个;B元素与A元素可组成一种淡黄色固体E;C的最高价氧化物既可以与酸反应,也可以和碱反应;D元素原子的M层上有7个电子。
(1)C元素的名称 ________;D的气态氢化物与H2S相比,稳定性较强的是_______(用化学式表示);
(2)A、B、C、D三种元素形成的简单离子半径由大到小的顺序为___________________(用化学式表示);
(3)A的常见氢化物中有两种,其中含有18个电子的分子的电子式为是______________。
(4)用电子式表示化合物B2A的形成过程__________________________。
(5)钾元素与B元素位于同一主族,钾元素与A元素可形成K2A、K2A2、KA2等多种化合物,其中K2A2和KA2和CO2均可发生反应(反应与淡黄色固体E和CO2的反应类似),写出K2A2与CO2发生反应的化学方程式_______________________________。
【答案】 铝 HCl Cl-> O2->Na+>Al3+ 略 Na2O形成过程(略) 2K2O2+2CO2==2K2CO3+O2
【解析】现有短周期A、B、C、D四种元素,它们的原子序数依次增大,A元素形成的-2价阴离子比氦原子的核外电子数多8个,A是O;B元素与A元素可组成一种淡黄色固体E,B是Na,E是过氧化钠;C的最高价氧化物既可以与酸反应,也可以和碱反应,C是Al;D元素原子的M层上有7个电子,核外电子数是17,D是Cl。则
(1)C元素的名称是铝;氯元素非金属性强于硫,则Cl的气态氢化物与H2S相比,稳定性较强的是HCl;(2)离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则A、B、C、D三种元素形成的简单离子半径由大到小的顺序为Cl-> O2->Na+>Al3+;(3)A的常见氢化物中有两种,其中含有18个电子的分子是双氧水,电子式为是![]() 。(4)氧化钠的形成过程为
。(4)氧化钠的形成过程为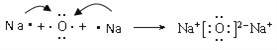 。(5)根据过氧化钠和二氧化碳的反应可判断K2O2与CO2发生反应的化学方程式为2K2O2+2CO2=2K2CO3+O2。
。(5)根据过氧化钠和二氧化碳的反应可判断K2O2与CO2发生反应的化学方程式为2K2O2+2CO2=2K2CO3+O2。


科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d、e为元素周期表中前4周期的一部分元素,下列有关叙述正确的是( )
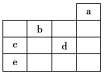
A. 元素b位于第ⅥA族,有+6、-2价两种常见化合价
B. 五种元素中,元素e的性质最稳定
C. 元素c和d的最高价氧化物对应的水化物的酸性:c>d
D. 元素c和e的气态氢化物的稳定性:c>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对热化学方程式![]() H2(g)+
H2(g)+![]() I2(g)══HI(g) ΔΗ=+26 kJ·mol-1的叙述中,正确的是
I2(g)══HI(g) ΔΗ=+26 kJ·mol-1的叙述中,正确的是
A.1 mol氢气和1 mol碘蒸气完全反应需要吸收26 kJ的热量
B.1个氢分子和1个碘分子完全反应需要吸收52 kJ的热量
C.1 mol H2(g)与1 mol I2(g)完全反应生成2 mol的HI气体需吸收52 kJ的热量
D.![]() mol H2(g)与
mol H2(g)与![]() mol I2(g)完全反应放出26 kJ的热量
mol I2(g)完全反应放出26 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是( )
电解质 | 非电解质 | 化合物 | |
A | H2SO4 | Cl2 | NaCl |
B | NaOH | 酒精 | N2 |
C | CuSO4 | 水银 | CO2 |
D | BaSO4 | 蔗糖 | KClO3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
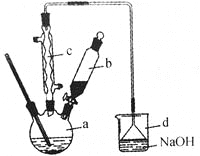
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g﹒cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须要做的是 (填入正确操作前的字母)
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于废弃塑料制品的处理方法中,最为恰当的是
A. 将废弃物焚烧 B. 将废弃物应用化学方法加工成防水涂料或汽油
C. 将废弃物倾倒在海洋中 D. 将废弃物切成碎片,混在垃圾中填埋于土壤中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于 aA(g)+bB(g)![]() cC(g)反应,改变某一变量(条件)得到如下图象(p 表示压强,T 表示温度,n 表示物质的量,á 表示平衡转化率)。根据图象,下列判断正确的是
cC(g)反应,改变某一变量(条件)得到如下图象(p 表示压强,T 表示温度,n 表示物质的量,á 表示平衡转化率)。根据图象,下列判断正确的是
A.反应 I:若 p1>p2,则 a+b<c
B. 反应Ⅱ:此反应的ΔH<0,且 T1<T2
C.反应Ⅲ:表示 t1 时刻一定是使用催化剂对反应速率的影响
D.反应Ⅳ:表示 t1 时刻增大 B 的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[ Na2C2O4 相对分子质量=134.0 ]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为: 5C2O42-+2MnO4-+16H+===10CO2↑+2Mn2++8H2O以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol/L的KMnO4溶液500mL。
步骤二:准确称取Na2C2O4固体mg放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配KMnO4溶液进行滴定。记录相关数据。
步骤三: 。
步骤四:计算得KMnO4溶液的物质的量浓度。
试回答下列问题:
(1)下左图为整个过程中可能使用的仪器的部分结构(有的仪器被放大),
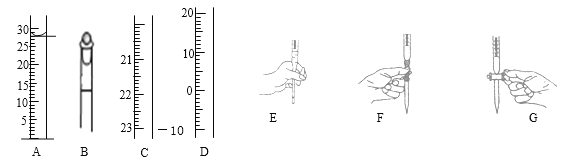
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量某液体的体积,平视时读数为NmL,仰视时读数为MmL,若M>N,则所使用的仪器是 (填字母标号)。
(2)该滴定实验滴定终点的现象是 。
(3)步骤二中滴定操作图示(上右图)正确的是 (填编号)。
(4)步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色中间明显变快,最后又变慢的原因是 。
(5)请写出步骤三的操作内容 。
(6)若m的数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为 mol/L。
(7)若滴定完毕后读数时俯视,则实验误差为 (填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定中和反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A. ①②③⑥ B. ①③④⑥ C. ③④⑤⑥ D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com