
| 序号 | 实验操作 | 现象 |
① | 向大试管中加入20mL 0.1mol?L-1的Na2S溶液 (已知Na2S溶液显碱性,pH约为12),再滴加5mL 0.1mol?L-1的FeCl3溶液,边滴边振荡 | 产生大量黑色沉淀,反应后溶液仍显碱性 |
② | 向另一支大试管中加入20mL 0.1mol?L-1FeCl3溶液(已知FeCl3溶液显酸性,pH约为2),再滴加5mL 0.1mol?L-1的Na2S溶液,边滴边振荡 | 局部有黑色沉淀但瞬间消失,溶液颜色变浅,并产生大量黄色浑浊,反应后溶液仍显酸性 |
| 实验操作 | 预期现象和结论 |
分析 (1)Fe3+与S2-的反应可能发生氧化还原反应,双水解反应,复分解反应;
(2)实验①发生的离子反应是铁离子和硫离子生成硫化物沉淀,实验②发生反应铁离子和硫离子发生氧化还原反应;
(3)取实验②所得混合液于试管中,滴入少量酸性KMnO4溶液,振荡,若酸性高锰酸钾紫色褪去,说明实验②中有Fe2+生成,取实验②所得混合物,过滤得到淡黄色的固体,取少量淡黄色的固体于试管中,滴加一定量的CS2振荡,淡黄色的固体溶解,说明实验②中有S生成;
(4)分析实验过程和实验现象可知,影响Fe3+与S2-的反应类型的可能因素是浓度、酸碱性和加入顺序;
解答 解:(1)猜想可能发生三种反应情况:双水解反应;氧化还原反应,
故答案为:复分解反应;
(2)实验①发生的离子反应是铁离子和硫离子生成硫化物沉淀,反应的离子方程式为:2Fe3++3S2-═Fe2S3↓,实验②发生反应铁离子和硫离子发生氧化还原反应,反应的离子方程式为:2Fe3++S2-═2Fe2++S↓,
故答案为:2Fe3++3S2-═Fe2S3↓,2Fe3++S2-═2Fe2++S↓;
(3)Fe2S3是黑色或深黄绿色固体,中性或碱性很稳定,FeS是黑褐色的固体,向另一支大试管中加入20mL 0.1mol?L-1FeCl3溶液(已知FeCl3溶液显酸性,pH约为2),再滴加5mL 0.1mol?L-1的Na2S溶液,边滴边振荡,局部有黑色沉淀但瞬间消失,溶液颜色变浅,并产生大量黄色浑浊,反应后溶液仍显酸性,设计实验验证是否含有亚铁离子,硫单质的检验方法,实验设计为:取实验②所得混合液于试管中,滴入少量酸性KMnO4溶液,振荡,若酸性高锰酸钾紫色褪去,说明实验②中有Fe2+生成,取实验②所得混合物,过滤得到淡黄色的固体,取少量淡黄色的固体于试管中,滴加一定量的CS2振荡,淡黄色的固体溶解,说明实验②中有S生成,
故答案为:
| 实 验 操 作 | 预期现象和结论 |
| 取实验②所得混合液于试管中,滴入少量酸性KMnO4溶液,振荡 | 若酸性高锰酸钾紫色褪去,说明实验②中有Fe2+生成 |
| 取实验②所得混合物,过滤得到淡黄色的固体,取少量淡黄色的固体于试管中,滴加一定量的CS2振荡 | 淡黄色的固体溶解,说明实验②中有S生成 |
点评 本题考查了离子性质,离子反应现象分析判断,注意实验设计的分析应用,掌握离子性质和存在的实验设计是解题关键,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | NO3-、Cl-、Fe3+、K+ | B. | Cl-、Ag+、NO3-、Na+ | ||
| C. | SO42-、Al3+、Na+、Cl- | D. | NO3-、HCO3-、Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
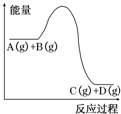
| A. | 加入催化剂时,该反应的反应热发生改变 | |
| B. | 升高温度,利于A的转化率增大 | |
| C. | 该反应的正反应为放热反应 | |
| D. | 增大压强,能够加快反应达到平衡状态的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol冰中有4NA个氢键 | |
| B. | 12克石墨中C---C键为2NA | |
| C. | 氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 | |
| D. | 六方最密堆积中,每个原子的配位数是12 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2SO4溶液中混有少量CuSO4的杂质可用适量的KOH除去 | |
| B. | Na2CO3固体中含有少量NaHCO3杂质可用加热的方法提纯 | |
| C. | Fe(NO3)3中混有少量Fe(NO3)2的杂质可加入适量的氯水除去 | |
| D. | 可以用分液的方法分离CCl4和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有⑤⑦ | C. | 只有③④⑥⑦ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com