
【题目】能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是
A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化硫气体
D.向水中加硫酸钠晶体
科目:高中化学 来源: 题型:
【题目】聚合物H ( )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:

已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels-Alder反应:![]() 。
。
(1)生成A的反应类型是_______。D的名称是_______。F中所含官能团的名称是_______。
(2)B的结构简式是_______;“B→C”的反应中,除C外,另外一种产物是_______。
(3)D+G→H的化学方程式是______。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有______种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的结构简式为______(任写一种)。
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成 ,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,同时产生黑烟
C.乙烯的结构简式为CH2=CH2
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是基础化工的重要产品,工业上制备硫酸的主要反应为:
造气: 4 FeS2 +11O2 ![]() 2 Fe2O3+ 8 SO2
2 Fe2O3+ 8 SO2
催化氧化: 2 SO2 + O2 ![]() 2 SO3
2 SO3
吸收: SO3 + H2O → H2SO4
完成下列填空:
(1)一定条件下,1 mol SO2和0.75 mol O2在容积为1 L的恒容密闭容器中发生反应,5 min时达到化学平衡。
①反应达到平衡后若改变条件使平衡常数K值变大,则在平衡移动过程中υ(正) _______(填序号)
a.一直增大 b.一直减小 c.先增大后减小 d.先减小后增大
②达到平衡时若SO3的浓度为0.98 mol·L-1,则5min内氧气的反应速率为_________ mol·L-1·min-1。反应体系中氧气过量的目的是_____________________。
(2)催化氧化反应中,SO2的平衡转化率与温度、压强的关系如图所示。则工业生产中最适宜的压强为___________,最适宜的温度范围为___________。

(3)若制取硫酸的上述三个反应过程中硫元素的转化率都是98%, 则1 mol硫铁矿可以制得SO2____________L(标准状况下),最终得到纯硫酸______________mol(均保留2位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是
2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是

A. 点a的正反应速率比点b的小
B. 点c处反应达到平衡
C. 点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D. 点e处反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的描述不正确的是( )
A. MgF2的电子式:![]()
B. 中子数为15的硅原子:![]()
C. 次氯酸的结构式:H—Cl—O
D. NH3·H2O的电离方程式:NH3·H2O![]() NH4++OH—
NH4++OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题。该小组设计的简单实验装置如图所示,该实验的主要操作步骤如下:
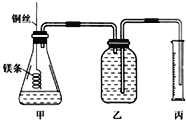
配制100ml1.0mol·L-1的盐酸溶液,用______(填仪器名称并注明规格)量取10.0ml1.0mol/L的盐酸溶液加入锥形瓶中;用托盘天平称取ag已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为_________;往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;反应结束后待体系温度恢复到室温,读出量筒中水的体积为VmL。
(1)请将上述步骤补充完整。
(2)用文字表述实验步骤④中检查装置气密性的方法:__________________________。
(3)实验步骤⑤中应选用_________(填序号)的量筒。
A.100ml B.200ml C.500ml
(4)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积Vm=_____________,若未除去镁条表面的氧化膜,则测量结果___________________(填“偏大”、“偏小”或“无影响”)。
(5)若在配制盐酸过程中出现下列情况,将使所配制的溶液的浓度偏高的是___________(填各选项的序号)。
a.配制溶液所用的容量瓶洗净后没有烘干
b.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
c.最后确定HCl溶液体积(定容)时,俯视观察液面与容量瓶刻度线
d.定容摇匀后静置,发现液面低于刻度线,再加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用麻醉药苄佐卡因E和食品防腐剂J的合成路线如下:
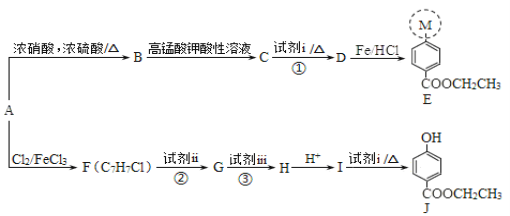
已知:I.M代表E分子结构中的一部分
II.![]()
请回答下列问题:
(1)A属于芳香烃,分子式为C7H8 ,其名称是_______,A到B的反应类型是______________________。
(2)E中所含含氧官能团的名称是_______,M的结构简式是__________。
(3)C能与NaHCO3溶液反应,则反应①的化学方程式是_____________。
(4)反应②、③中试剂ii和试剂iii依次是_______。(填序号)
a.高锰酸钾酸性溶液、氢氧化钠溶液
b.氢氧化钠溶液、高锰酸钾酸性溶液
(5)H的结构简式是_______。
(6)J有多种同分异构体,其中符合下列条件的同分异构体有______ 种,写出其中任一种同分异构体的结构简式:____。
a.为苯的二元取代物
b.遇到FeCl3溶液显紫色,能发生水解反应且能发生银镜反应
(7)以A为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(![]() ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):_____________
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com