
 3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )
3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )| A.C和D可能都是固体 |
| B.C和D一定都是气体 |
| C.若D为固体,则C一定是气体 |
| D.C和D可能都是气体 |
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:不详 题型:填空题
 2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | t |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是
N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是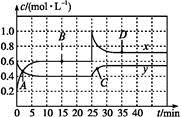
| A.图中共有两条曲线x和y,其中曲线y表示NO2浓度随时间的变化 |
| B.A、B、C、D四个点中,表示化学反应处于平衡状态的点是B和C |
| C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4 |
| D.若要达到与D相同的状态,在25 min时还可采取的措施是适当缩小容器体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1。在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1。在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。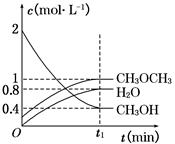
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)
2NH3(g)| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
 N2(g)+3H2(g)的化学平衡常数K的值为________,当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“>”“<”或“=”)
N2(g)+3H2(g)的化学平衡常数K的值为________,当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“>”“<”或“=”)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是
TaI4(g)+S2(g) △H>0。t min时生成0.1 mol TaI4。下列说法正确的是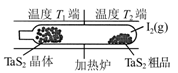
A.0~t min内,v(I2)=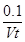 mol·L-1·min-1 mol·L-1·min-1 |
| B.若T℃时反应的平衡常数K=1,则平衡时I2的转化率为2/3 |
| C.如图制备TaS2晶体过程中循环使用的物质是S2(g) |
| D.图中T1端得到纯净TaS2晶体,则温度T1<T2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+D(g)达到平衡后,升高温度容器
C(g)+D(g)达到平衡后,升高温度容器| A.正反应是放热反应 |
| B.A不是气态物质,加入A该平衡向正反应方向移动 |
| C.其他条件不变,加入A平衡不移动 |
| D.改变压强对该平衡的移动无影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3达到平衡的标志是( )。
2SO3达到平衡的标志是( )。| A.①② | B.①③ | C.③ | D.① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com