
试计算25℃时(Kw=1×10﹣14),50mL0.005mol/LH2SO4中:
(1)c(H+)=?
(2)求该H2SO4溶液的pH值.
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
现有CO、CO2和O3三种气体,它们都含有1摩尔氧原子,则三种气体的物质的量之比为( )
|
| A. | 1:1:1: | B. | 1:2:3 | C. | 3:2:1 | D. | 6:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | PH小于7时一定为酸性 |
|
| B. | 水离子积Kw与 温度、酸碱性有关 |
|
| C. | c(H+)=c(OH﹣)的溶液一定为中性溶液 |
|
| D. | 加入酸或碱促进水电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)⇌2AB2(g)(正反应放热),下列说法正确的( )
|
| A. | 升高温度,正向反应速率减小,逆向反应速率增加 |
|
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
|
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
|
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于强弱电解质及非电解质的组合完全正确的是( )
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | 氨水 | HClO | HI |
| 非电解质 | Cl2 | 蔗糖 | C2H5OH | SO2 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯水加热至较高温度,下列叙述正确的是( )
|
| A. | 水的离子积变大、pH变小、呈酸性 |
|
| B. | 水的离了积不变、pH不变、呈中性 |
|
| C. | 水的离子积变小、pH变大、呈碱性 |
|
| D. | 水的离子积变大、pH变小、呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知元素X的基态原子最外层电子排布为nsn﹣1npn+2,则它最高价氧化物对应的水化物的酸根离子是( )
|
| A. | RO | B. | RO43﹣ | C. | RO | D. | RO32﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某条件下,在2 L密闭容器中发生如下反应:2NO2(g)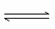 2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800 ℃,实验Ⅲ在850 ℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800 ℃,实验Ⅲ在850 ℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:

(1)实验Ⅱ隐含的反应条件是 。
(2)实验II中,从反应开始至达到平衡,用氧气浓度变化表示的化学反应速率为 。
(3)800 ℃时,该反应的平衡常数K= 。该反应是 (填“吸” 或“ 放”)热反应。
(4)若实验Ⅰ中达到平衡后,再向密闭容器中通入2 mol由物质的量之比为1∶1组成的NO2与O2混合气体(保持温度不变),此时反应将向 (填“正反应”或“逆反应”)方向进行。
(5)NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转化为无害的参与大气循环的物质,如:8NH3+6NO2 7N2+12H2O。若将此反应设计成原电池,融熔K2CO3为电解质,则正极反应方程式为: 。
7N2+12H2O。若将此反应设计成原电池,融熔K2CO3为电解质,则正极反应方程式为: 。
(6)向AlCl3溶液中逐滴加入氨水,发生如下反应Al3++3NH3·H2O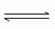 Al(OH)3↓+3
Al(OH)3↓+3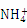 ,一般认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时,沉淀已完全。已知当溶液中Al3+恰好沉淀完全时溶液的pH=4.7,则Al(OH)3的溶度积常数为 (已知:lg2=0.3)。
,一般认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时,沉淀已完全。已知当溶液中Al3+恰好沉淀完全时溶液的pH=4.7,则Al(OH)3的溶度积常数为 (已知:lg2=0.3)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com