
【题目】《本草纲目拾遗》中在药物名“鼻冲水”条目下写到:“贮以玻璃瓶,紧塞其口,勿使漏气,则药力不减。气甚辛烈,触人脑,非有病不可嗅”。这里所说的“鼻冲水”指的是
A. 稀硝酸 B. 食醋 C. 氨水 D. 氢氟酸
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案科目:高中化学 来源: 题型:
【题目】反应4NH3+5O2 ![]() 4NO+6H2O(g)在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则下列反应速率正确的是 ( )
4NO+6H2O(g)在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则下列反应速率正确的是 ( )
A. V(O2)=0.01mol ·L-1 ·s-1 B. V(NO)=0.008mol ·L-1 ·s-1
C. V(H2O)=0.015mol ·L-1 ·s-1 D. V(NH3)=0.002mol ·L-1 ·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行氯气的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是

① | ② | ③ | ④ | |
A | 黄绿色 | 橙色 | 蓝色 | 无色 |
B | 无色 | 橙色 | 紫色 | 白色 |
C | 黄绿色 | 橙色 | 蓝色 | 白色 |
D | 黄绿色 | 无色 | 紫色 | 白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3 和MgSO4 的混合溶液中,滴加NaOH 溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中 Al2(SO4)3 与MgSO4 的物质的量浓度之比为( )
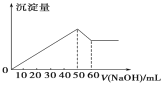
A. 1∶2 B. 2∶1 C. 6∶1 D. 3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用如下图的表示方法形象地表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的是 ( )

A. ①②③为同种核素
B. ①②③互为同位素
C. ①②③是三种化学性质不同的粒子
D. ①②③三种的质量数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称。丝绸是一种天然高分子材料。下列不属于高分子物质的是
A. 纤维素 B. 植物油 C. 聚乙烯 D. 蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。
(1)工业上的湿法制备方法是用KClO与Fe(OH)3在KOH存在下制得K2FeO4,该反应氧化剂与还原剂物质的量之比为____________。
(2)实验室用食盐、废铁屑、硫酸、KOH等为原料,通过以下过程制备K2FeO4:

①操作(Ⅰ)的方法为_______________,隔绝空气减压干燥。
②检验产生X气体的方法是_____________。
③最终在溶液中得到K2FeO4晶体利用的原理是_____________。
(3)测定某K2FeO4样品的质量分数,实验步骤如下:
步骤1:准确称量1.0g样品,配制100mL溶液;
步骤2:准确量取25.00mL K2FeO4溶液加入到锥形瓶中;
步骤3:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-;
步骤4:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤5:加入二苯胺磺酸钠作指示剂,用0.1000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显紫红色),记下消耗(NH4)2Fe(SO4)溶液的体积,做3次平行实验,平均消耗30.00 mL的(NH4)2Fe(SO4)2溶液。
已知:滴定时发生的反应为:6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O。
①步骤2中准确量取25.00mL K2FeO4溶液加入到锥形瓶中所用的仪器是________。
②写出步骤3中发生反应的离子方程式________________________。
③步骤5中能否不加指示剂______(填“能”或“否”),原因是___________。
④根据上述实验数据,测定该样品中K2FeO4的质量分数为__________。
(4)配制0.1mol·L-1的K2FeO4,调节溶液pH,含铁离子在水溶液中的存在形态如图所示。下列说法正确的是_________(填字母)。

A.pH=2时,c(H3FeO4+)+c(H2FeO4)+c(HFeO4-)=0.1mol·L-1
B.向pH=10的这种溶液中加硫酸铵,则HFeO4-的分布分数逐渐增大
C.向pH=1的溶液中加HI溶液,发生反应的离子方程式为:H2FeO4+H+==H3FeO4+
D.将K2FeO4晶体溶于水,水溶液呈弱碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属粉末的混合物15 g,投入足量的稀盐酸中,得到5.6 L氢气(标准状况),则这种混合物可能是
A. 镁和铁 B. 镁和铝 C. 铁和锌 D. 铜和锌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com