

| A. | 苯环上的一氯代物种数相同 | |
| B. | 分子中共面的碳原子数一定相同 | |
| C. | 1 mol甲与浓溴水反应最多能消耗4 mol Br2 | |
| D. | 甲、乙可用红外光谱区分,但不能用核磁共振氢谱区分 |
分析 A.甲中苯环上有5种氢原子,所以其苯环上的一氯代物有5种;乙苯环上有4种,其苯环上一氯代物有4种;
B.甲中分子共平面的碳原子最少有9个、最多有15个,乙中共平面的碳原子最多15个、最少8个;
C.甲中能和溴反应的有碳碳双键和苯环上酚羟基的邻对位氢原子;
D.甲、乙官能团不同且氢原子种类不同.
解答 解:A.甲中苯环上有5种氢原子,所以其苯环上的一氯代物有5种;乙苯环上有4种,其苯环上一氯代物有4种,所以苯环上的一氯代物种数不同,故A错误;
B.甲中分子共平面的碳原子最少有9个、最多有15个,乙中共平面的碳原子最多15个、最少8个,所以分子中共面的碳原子数不一定相同,故B错误;
C.甲中能和溴反应的有碳碳双键和苯环上酚羟基的邻对位氢原子,所以1 mol甲与浓溴水反应最多能消耗4 mol Br2,故C正确;
D.甲、乙官能团不同且氢原子种类不同,所以可以用红外光谱、核磁共振氢谱区分,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断及空间想象能力,明确官能团及其结构性质关系是解本题关键,易错选项是B.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:解答题
 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下: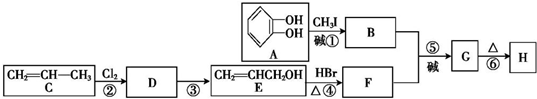
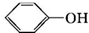 +RX$\stackrel{碱}{→}$
+RX$\stackrel{碱}{→}$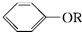 +HX(X代表卤素原子);
+HX(X代表卤素原子);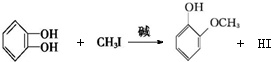 .
.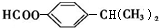 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
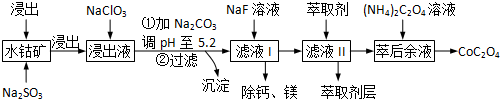
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
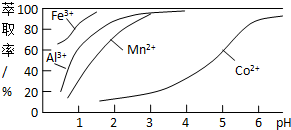
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | Q |
| A. | Y 的非金属性比Q强,所以HnY的酸性比HnQ强 | |
| B. | ZX2、WX2的熔沸点、硬度相差很大,这是由于它们的化学键类型不同造成的 | |
| C. | W、Q、Y 元素的原子半径及其简单离子半径依次减小 | |
| D. | 将足量的 X 单质通入 W 的氢化物的水溶液,能得到 W 的低价氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:H2O>NH3 | B. | 碱性:NaOH>Al(OH)3 | ||
| C. | 氧化性:F2>Cl2 | D. | 酸性:CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:MnO2>SO42->IO3->I2 | |
| B. | I2在反应①中是还原产物,在反应②中是氧化产物 | |
| C. | 反应①②中生成等量的I2时转移电子数之比为1:5 | |
| D. | NaHSO3溶液呈酸性,NaHSO3溶液中c(HSO3-)>c(H2SO3)>c(SO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3的分解过程中只有共价键断裂没有共价键生成 | |
| B. | 火药爆炸会使周围空气体积迅速膨胀 | |
| C. | 若白磷完全燃烧释放出8akJ热量,则需要标准状况下的O2体积为224L | |
| D. | 易燃易爆物应远离火源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com