
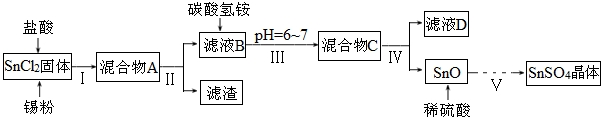
分析 由于Sn2+易水解、易被氧化,加入盐酸,抑制Sn2+水解,加入Sn粉可以与盐酸反应,调节溶液pH,还防止Sn2+被氧化,步骤Ⅱ为过滤,得SnCl2溶液,向其中加碳酸氢铵,调节溶液pH=6-7,使Sn元素以SnO形式沉淀,再过滤洗涤得纯净的SnO,加稀硫酸,得SnSO4溶液,蒸发浓缩、冷却结晶、过滤、洗涤,制得SnSO4晶体,滤液D中含有大量的NH4Cl等,据此分析;
(1)①加入盐酸,抑制Sn2+水解;
②步骤Ⅱ为过滤;沉淀为SnO表面附着着Cl-,要想检验滤渣是否洗涤干净,用硝酸、硝酸银溶液检验最后一次洗涤液中是否含有Cl-;
③步骤Ⅴ是用硫酸溶解后,从溶液中获得晶体,滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,制得SnSO4晶体;
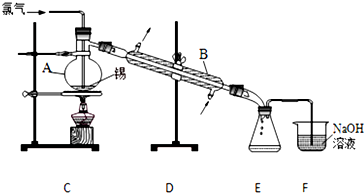
(2)①仪器B的名称为冷凝管;
②由信息可知SnCl4遇水水解,F中氢氧化钠溶液中水蒸气易挥发进入E中;
③根据产率=实际产量理论产量×100%,据此解答即可.
解答 解:(1)①加入盐酸,抑制Sn2+水解,故答案为:抑制Sn2+水解;
②步骤Ⅱ为过滤,用到的玻璃仪器除烧杯外还有漏斗、玻璃棒,
沉淀为SnO表面附着着Cl-,要想检验滤渣是否洗涤干净,用硝酸、硝酸银溶液检验最后一次洗涤液中是否含有Cl-,具体方案为:取最后一次洗涤液,加入硝酸酸化的硝酸银,如果没有出现沉淀,说明洗涤干净,如果出现沉淀,说明没有洗涤干净;故答案为:漏斗、玻璃棒;取最后一次洗涤液,加入硝酸酸化的硝酸银,如果没有出现沉淀,说明洗涤干净,如果出现沉淀,说明没有洗涤干净;
③步骤Ⅴ是用硫酸溶解后,从溶液中获得晶体,滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,制得SnSO4晶体,故答案为:冷却结晶;过滤;
(2)①仪器B为冷凝管,又称为冷凝器,故答案为:冷凝管;
②E收集产品,F中氢氧化钠溶液中水蒸气易挥发,进入E中,易使SnCl4水解.在E和F之间增加干燥装置可以避免此种情况发生,故答案为:E、F之间连装有碱石灰的干燥管;
③11.9gSn粉的物质的量为:11.9g119g/mol=0.1mol,故应生成SnCl4极的物质的量为0.1mol,即质量为:0.1mol×(119+4×35.5)g/mol=26.1g,产率=23.8g26.1g×100%≈91.2%,故答案为:91.2%.
点评 本题主要考查的是制备实验方案的设计,综合性较强,难度较大,涉及知识点:实验室常见仪器、盐类水解原理、氧化还原反应原理等,充分利用所给信息是解决本题的关键.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 10ml | B. | 5ml | C. | 大于5ml | D. | 小于5ml |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
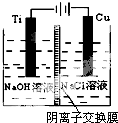 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O; |
| 方法c | 电解法,反应为2Cu+H2O电解_Cu2O+H2↑. |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
| 序号 | 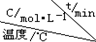 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
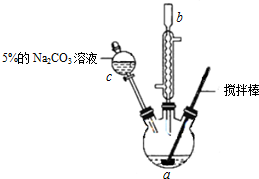
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 密度 | 沸点 | 溶解性 | ||
| 丙烯酸 | 1.05g/cm3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 0.79g/cm3 | 64.7℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 0.95g/cm3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
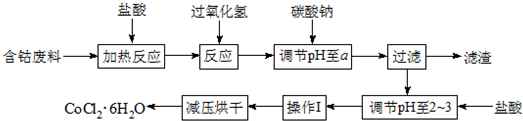
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测HCl溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧具有氧化性,可用作自来水的消毒剂 | |
| B. | 活性炭具有还原性,可用作制糖业脱色剂 | |
| C. | 氢氟酸具有弱酸性,可用作玻璃的蚀刻剂 | |
| D. | 氨气具有弱碱性,可用作食品工业制冷剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com