
【题目】(1)![]() 的放射性可用于考古断代,根据测定出土文物标本中
的放射性可用于考古断代,根据测定出土文物标本中![]() 的含量,就可以推算出文物的年代。
的含量,就可以推算出文物的年代。![]() 的中子数是______________。
的中子数是______________。
(2)碘元素的一种核素12553I可用于治疗肿瘤。该核素的质子数为__________,中子数为_____________,质量数为____________。
(3)写出铝原子的原子结构示意图___________________。
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量氢氧化钠溶液;③加适量盐酸;④加过量碳酸钠溶液;⑤加过量氯化钡溶液。下列操作顺序正确的是
A.⑤②④①③B.④①②⑤③
C.④②⑤①③D.①④②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下: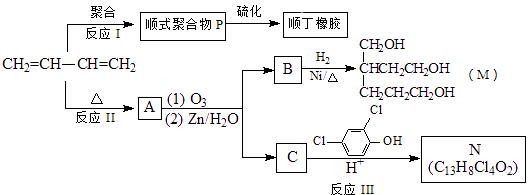
已知:i. 
ⅱ.RCH=CHR′ ![]() RCHO+R′CHO (R、R′代表烃基或氢)
RCHO+R′CHO (R、R′代表烃基或氢)
(1)CH2=CH﹣CH=CH2的名称是 .
(2)反应Ⅰ的反应类型是(选填字母) .
a、加聚反应 b、缩聚反应
(3)顺式聚合物P的结构式是(选填字母) . 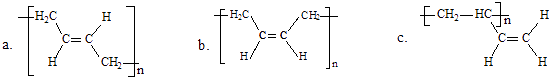
(4)A的相对分子质量为108.
①反应Ⅱ的化学方程式是 .
②1mol B完全转化成M所消耗H2的质量是g.
(5)反应Ⅲ的化学方程式是 .
(6)A的某些同分异构体在相同的反应条件下也能生成B和C,写出其中一种同分异构体的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组得到一块软锰矿样品,其主要成分为二氧化锰( MnO2)和石英(SiO2)。为了制取Cl2和探究氯及其化合物的相关性质,进行如下实验。
【查阅资料】MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
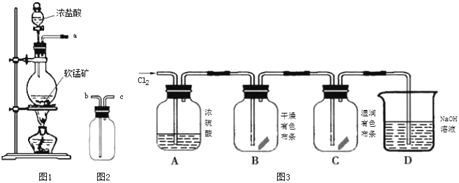
【制取气体】
(1)取适量矿样置于烧瓶中,加入足量浓盐酸并加热,充分反应后烧瓶中残留的固体是____。
(2)收集氯气应将图1导管的a接口与图2导管的_____________接口连接(填“b”或“c)。
(3)已知氯气中含有HCl杂质,可用______________除去。
【实验探究】
(4)把红热的铁丝伸入盛有氯气的集气瓶中,铁丝燃烧产生棕褐色的烟。反应的化学方程式是_______________________________________________________________________。
(5)按图3进行实验,观察到B中的有色布条不褪色,C中的有色布条褪色。由此得出的结论是_____________________________________________________________________。
(6)写出C中反应的化学方程式:_________________________________________________。
【联系实际】
(7)某氯碱工厂的氯气管道发生泄漏,以下采取的措施正确的是______________ (双项选择,填序号)。
A.将人群向高处疏散
B.将人群向低处疏散
C.关闭氯气管道,用碱液浸泡过的棉布覆盖泄漏部位
D.关闭氯气管道,用饱和NaCl溶液浸泡过的棉布覆盖泄漏部位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示。

(1)写出圆底烧瓶中发生反应的离子方程式
____________________________________________________。
(2)如果将过量二氧化锰与20mL12mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①__________________________________,
②________________________________________。
(3)为了提高浓盐酸的利用率,你对该实验的建议是_________。
(4)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是____________________,有关的离子方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于Cl2对饮用水消毒,生成的有机氯化物对人体有害。世界环保联盟建议使用ClO2,它是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:KClO3+H2C2O4+H2SO4—— ClO2↑+K2SO4+CO2↑+H2O(未配平)。下列说法正确的是( )
A. KClO3在反应中是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的约5.3倍
D. 1 mol KClO3参加反应有1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下: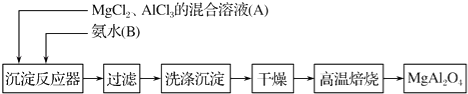
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为 .
(2)判断流程中沉淀是否洗净所用的试剂是 .
(3)在25℃下,向浓度均为0.01mol/L的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式: .
【已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Al(OH)3]=3×10﹣34】
(4)将Mg、Al组成的9.9g混合物投入一定量稀硝酸中,恰好完全反应,共收集到还原产物NO气体6.72L(标准状况),向反应后的溶液中加入4mol/L的Na0H溶液300mL时,则形成沉淀的质量为g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com