
| A. | 卤素单质与水反应的通式为X2+H2O═HX+HXO | |
| B. | HX都极易溶于水,它们的稳定性随核电荷数的增加而增强 | |
| C. | 卤素单质的颜色随相对分子质量的增大而加深 | |
| D. | X2的氧化性随核电荷数的增加而增强 |
分析 A.氟气和水反应生成HF和氧气;
B.卤族元素的非金属性越强,其氢化物越稳定;
C.卤族元素单质随着原子序数的增大而逐渐加深;
D.元素的非金属性越强,其单质的氧化性越强;
解答 解:A.氟气和水反应生成HF和氧气,氯气、溴、碘单质与水反应均可用X2+H2O═HXO+HX表示,故A错误;
B.卤族元素的非金属性越强,其氢化物越稳定,卤族元素氢化物都易溶于水,但它们的热稳定性随核电荷数增大而减弱,故B错误;
C.卤族元素单质随着原子序数的增大而逐渐加深,所以卤素单质从F2→I2颜色逐渐加深,故C正确;
D.元素的非金属性越强,其单质的氧化性越强,非金属性强弱F>Cl>Br>I,所以卤素单质的氧化性随核电荷数的增加而减弱,故D错误;
故选C.
点评 本题考查了卤族元素性质的递变规律,知道其规律中的异常现象即可解答,知道氟气和水的反应产物,卤族元素氢化物中HF为弱酸,盐酸、氢溴酸、氢碘酸都是强酸,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 5(b+2a-c) | B. | $\frac{5(2b-c)}{3}$ | C. | $\frac{5(2b-a+c)}{3}$ | D. | 5(b-c) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
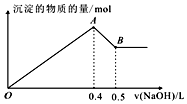 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 6:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 2:1:1 | C. | 3:1:1 | D. | 1:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素所在族序数的二倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C依次是( )
短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素所在族序数的二倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C依次是( )| A. | Be、Na、Al | B. | C、Al、P | C. | O、P、Cl | D. | B、Mg、S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com