
| A、平衡向逆反应方向移动了 |
| B、x+y>z |
| C、B的转化率下降 |
| D、C的体积分数减小 |


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案科目:高中化学 来源: 题型:
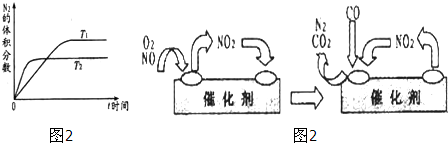
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用完的电池可以随意地丢弃 |
| B、增加炼铁高炉的高度可以降低尾气中CO的含量 |
| C、加入正催化剂是能大大提高化学反应速率 |
| D、把煤粉碎了再燃烧不可以提高煤的燃烧效率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com