
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和(CuSO4) |
| ④将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡,铜片上不产生气泡 |
| ⑤将铁片和铜片同时插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 金属的金属性强弱判断方法:金属的金属性越强,其最高价氧化物的水化物碱性越强,活泼性较强的金属能置换出较不活泼金属,金属和酸或水反应越剧烈,据此分析解答.
解答 解:金属的金属性强弱判断方法:金属的金属性越强,其最高价氧化物的水化物碱性越强,活泼性较强的金属能置换出较不活泼金属,金属和酸或水反应越剧烈,
①将铁片置于CuSO4溶液中,铁片上有亮红色物质析出,Fe能置换出硫酸铜中的铜,说明金属性铁>铜,故正确;
②将铁丝和铜丝分别在氯气中燃烧,产物分别为FeCl3和CuCl2,Fe元素化合价变化大于Cu,不能根据金属失电子多少判断金属性强弱,故错误;
③将铁片和铜片分别放入热浓硫酸中产物分别为Fe2(SO4)3和CuSO4,Fe元素化合价变化大于Cu,不能根据金属失电子多少判断金属性强弱,故错误;
④将铁片和铜片分别置于稀硫酸溶液中,铁片上有气泡,铜片上不产生气泡,说明金属性Fe>Cu,故正确;
⑤将铁片和铜片同时插入盛有稀硫酸的烧杯中,并用导线连接,铁片溶解,铜片上有气泡产生,说明Fe能置换出氢气、铜不能置换出氢气,则金属性Fe>Cu,故正确;
故选B.
点评 本题考查金属性强弱判断方法,明确金属性强弱与金属失电子难易程度有关,与失电子多少无关,为易错题.


科目:高中化学 来源: 题型:选择题
| A. | 溶液pH由大变小 | B. | 负极附近Zn2+浓度逐渐增大 | ||
| C. | H+向负极移动 | D. | 溶液中H2SO4的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  铁丝的析氢腐蚀实验 | B. | 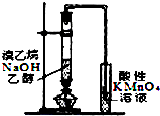 检验该反应的有机产物 | ||
| C. | 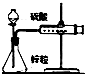 结合秒表测量锌与硫酸的反应速率 | D. | 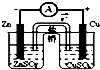 验证化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水 氯水 碘水 | B. | 氢溴酸 盐酸 氢硫酸 | ||
| C. | 浓硫酸 浓硝酸 浓盐酸 | D. | NaOH溶液 Na2CO3溶液 水玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的HNO2溶液中[H+]约为0.01 mol•L-1 | |
| B. | 用HNO2溶液做导电实验,灯泡很暗 | |
| C. | HNO2溶液不与Na2SO4溶液反应 | |
| D. | HNO2能与NaOH溶液发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往NaOH溶液中通入过量CO2:CO2+OH-═HCO3- | |
| B. | 往水玻璃中加入盐酸:SiO32-+2H+═H2SiO3↓ | |
| C. | 石英砂与烧碱反应制水玻璃:SiO2+2OH-═SiO32-+H2O | |
| D. | 往水玻璃中通入CO2:Na2SiO3+H2O+CO2═H2SiO3+2Na++CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com