
【题目】(1)写出2,2-二甲基-3-乙基戊烷的结构简式___;
(2)写出蔗糖的分子式___;
(3)医院常用消毒酒精的体积分数是___;
(4)乙酸乙酯在酸性条件下水解的化学方程式___。
【答案】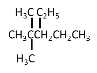 或(CH3)3CCH2(C2H5)2 C12H22O11 75% CH3COOC2H5+H2O
或(CH3)3CCH2(C2H5)2 C12H22O11 75% CH3COOC2H5+H2O![]() CH3COOH+C2H5OH
CH3COOH+C2H5OH
【解析】
(1) 2,2-二甲基-3-乙基戊烷的结构简式为: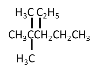 或(CH3)3CCH2(C2H5)2,故答案为:
或(CH3)3CCH2(C2H5)2,故答案为: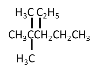 或(CH3)3CCH2(C2H5)2;
或(CH3)3CCH2(C2H5)2;
(2)蔗糖的分子式为:C12H22O11,故答案为:C12H22O11;
(3)医院常用体积分数75%的酒精消毒,故答案为:75%;
(4)乙酸乙酯在酸性条件下水解生成乙酸和乙醇,化学方程式为;CH3COOC2H5+H2O![]() CH3COOH+C2H5OH,故答案为:CH3COOC2H5+H2O
CH3COOH+C2H5OH,故答案为:CH3COOC2H5+H2O![]() CH3COOH+C2H5OH。
CH3COOH+C2H5OH。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】1500C、1.0×105Pa时,aL乙炔,aL甲烷和aL丙烯的混合气体与过量的bLO2混合,点燃使这两种烃充分燃烧后,再恢复到原状况,此时混合气体的体积为
A. 10aL B. (3a+b)L C. (b-a)L D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯为原料,在一定条件下可以转化为A、B、C,最后合成有机化合物D,转化关系如下图所示:

请回答:
(1)写出有机物B的官能团名称:________________。
(2)写出CH3=CH2→A化学方程式:________________。
(3)有机化合物D的相对分子质量为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。

(1)B装置的作用是__________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中定有______气体产生,写出D中发生反应的离子方程式__________。若去掉C,是否能得出同样结论并解释其原因_____________。
(3)A中固体完全分解后变为红宗色粉末,某同学设计实验验证固体残留物仅为Fe2O3.而不含FeO。请完成表内容。(试剂,仅然和用品自选)
实验步骤 | 预期现象 | 结论 |
取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解:_________ | ___________ | 固体残留物仅为Fe2O3 |
(4)E中收集到的气体只有N2,其物质的量为xmol,固体残留物刚体死目物Fe2O3的物质的量为ymol,D中沉淀物质的量为zmol,根据氧化还原反应的基本规律,x、y和z应满足的关系为________。
(5)结合上述实验现象和相关数据的分析。写出硫酸亚铁铵在500℃时隔绝空气加热完全分解的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是镁-空气燃料电池工作原理示意图,电池总反应为2Mg+O2+2H2O=2Mg(OH)2。下列有关该电池的说法正确的是( )
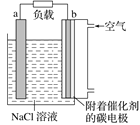
A.a极为负极,发生还原反应
B.b电极上电极反应:O2+2H2O+4e-=4OH-
C.工作时电子由b极经外电路流向a极
D.该装置实现了电能转化成化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
(1)用C表示10s内反应的平均反应速率为___;
(2)A与B的平衡转化率之比为___;
(3)反应过程中容器内气体的平均相对分子质量变化是___(填“增大”、“减小”或“不变”,下同),气体的密度变化是___;
(4)一定能说明上述反应已经达到化学平衡状态的是___。
a.容器内气体压强不再改变
b.2v(A)=3v(C)
c.A的浓度不再改变
d.A、B、C、D的分子数之比为3∶1∶2∶2
e.反应停止,不再继续进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。试回答下列问题:

(1)氢气进入的这极为___极;
(2)写出氢氧燃料电池工作时的正极反应式:___;
(3)该氢氧燃料电池每转移0.1mol电子,消耗标准状态下___L氧气;
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯是工业上重要的原料,是合成有机物的中间体。
2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0
2ClNO(g) △H<0
(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1 ,则平衡后NO的转化率α1=_____________。其它条件保持不变,反应在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”)。
(2)若使反应2NO(g)+Cl2(g)![]() 2ClNO(g) 的平衡常数增大,可采用的措施是___________。
2ClNO(g) 的平衡常数增大,可采用的措施是___________。
(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g)![]() 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。

(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
容器编号 | 温度/℃ | 容器体积/L | 平衡时ClNO含量(占比) |
Ⅰ | T1 | 2 | 2/3 |
Ⅱ | T2=T1 | 3 | W2 |
Ⅲ | T3>T1 | V3 | 2/3 |
Ⅳ | T4 | V4 | W4 |
Ⅴ | T5 | V5 | W5 |
①V3________2 (填写“大于”、“小于”或“等于”);
②容器Ⅱ中化学平衡常数K=_________;
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是_____________________;容器Ⅴ与容器Ⅰ的体积不同,则容器Ⅴ中反应达到平衡时气体总压强(P )的范围是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积固定的密闭容器中发生可逆反应4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)下列能说明反应已经达到平衡状态的是( )
A.混合气体的密度保持不变
B.混合气体的平均相对分子质量保持不变
C.断开4molH﹣Cl键的同时,生成4molH﹣O键
D.HCl、O2、H2O、Cl2四种气体的物质的量之比为4:1:2:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com