
| A. | 维生素C具有还原性,能在人体内起抗氧化作用 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 糖类是产生能量最高的营养物质 | |
| D. | 废电池必须进行集中处理的首要原因是回收利用石墨电极和金属材料 |
分析 A.维生素C具有还原性,能防止亚铁离子氧化;
B.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染;
C.基本营养物质有糖类、油脂、蛋白质等,其中单位质量的油脂产生的能量最高;
D.废旧电池中含有重金属离子.
解答 解:A.维生素C具有还原性,能防止亚铁离子氧化,则能在人体内起抗氧化作用,故A正确;
B.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,而不能污染后再治理,故B错误;
C.基本营养物质有糖类、油脂、蛋白质等,其中单位质量的油脂产生的能量最高,而不是糖类,故C错误;
D.废旧电池中含有重金属离子,会污染土壤及地下水,而回收利用石墨电极和金属材料不是首要原因,故D错误;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应及用途为解答的关键,侧重分析能力与应用能力的考查,注意化学与生活、环境的关系,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 5% | B. | 9.1% | C. | 10.5% | D. | 15.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂 | 方法 |
| A | 分离碘水中的碘 | 乙醇 | 萃取 |
| B | 分离乙酸乙酯和乙醇 | 氢氧化钠溶液 | 分液 |
| C | 除去乙醇中乙酸 | 氧化钙 | 蒸馏 |
| D | 除去乙烷中的乙烯 | 溴的四氯化碳溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑥ | B. | ①③④⑥ | C. | ②④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
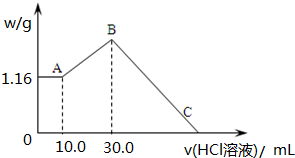
 将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题:
将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-Fe3+ Na+ | B. | Al3+Ba2+HCO3- | C. | K+Na+CO32- | D. | NH4+K+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.5倍 | |
| B. | 若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量这比为2:1 | |
| C. | 若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 | |
| D. | 平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com