
| A、25℃时,pH=12的1.0 L NaClO溶液中水电离出OH-的数目为0.01 NA |
| B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA |
| C、0.1 mol乙醇中含有0.6 NA个C-H共价键 |
| D、常温、常压下,3.5 g 35Cl2所含中子数为0.1 NA |


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、17 g NH3中含有的质子数为1 mol |
| B、同温同压下CO与N2气体密度相同 |
| C、20 g CuSO4?5H2O溶于80 g水所得溶液溶质质量分数为20% |
| D、16 g CH4在标准状况下体积为 11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2和T2 互为同素异形体 | ||||
B、
| ||||
| C、乙醇和二甲醚互为同分异构体 | ||||
| D、苯和甲苯互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
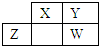 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )
四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )| A、X、Y、Z、W均为非金属元素 |
| B、X、Y、W的氢化物中,Y的氢化物沸点最高 |
| C、Z的阳离子与Y的阴离子电子层结构相同 |
| D、W元素的简单离子半径大于Z元素的简单离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分散质微粒能透过半透膜 |
| B、是不稳定的分散系 |
| C、该胶体带电,带正电荷 |
| D、滴加入盐酸至过量,先产生红褐色沉淀,然后溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝表面易形成一层致密的氧化膜保护层,所以铝要以广泛用来制造炊具和包装食品 |
| B、制备氢氧化铁胶体是将FeCl3饱和溶液滴入沸水中并煮沸至红褐色 |
| C、向试管中滴加液体时,胶头滴管都不能伸入试管中 |
| D、金属钠﹑镁等活泼金属着火时,不能用直接用水灭火,而要用干粉灭火器灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A、当容器中气体的密度不变时,说明该反应已达到平衡状态 |
| B、用O2表示0~4 min内该反应的平均速率为0.005 mol/(L?min) |
| C、若升高温度,则SO2的反应速率会变大,平衡常数K值会增大 |
| D、平衡时再通入18O2,平衡右移,再次平衡时各物质均含有18O,O2的转化率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com