
| ① | ② | ③ | ④ |
| 0.1mol/L NaOH溶液 | pH=11 NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3 CH3COOH溶液 |
| A、由水电离出的c(H+):①>③ |
| B、③稀释到原来的100倍后,pH与④相同 |
| C、②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为:c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D、①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH) |


科目:高中化学 来源: 题型:
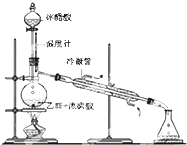 有机化学知识在生活中应用广泛.
有机化学知识在生活中应用广泛.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、倾倒液体时试剂瓶上的标签握在手心 |
| B、称量药品时用手取砝码 |
| C、稀释浓硫酸时将水倒入浓硫酸中 |
| D、用燃着的酒精灯去点燃另一酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳氢化合物 | B、二氧化碳 |
| C、可吸入颗粒物 | D、氮氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨是生产氮肥的重要原料 |
| B、磷肥和钾肥可从无机盐中获得 |
| C、大力推广有机氯、有机磷等有机合成农药 |
| D、开发使用高效、低毒、低残留的第三代环境友好型农药 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液滴入到足量的氨水中:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| B、碳酸氢钙溶液中加入少量苛性钾溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| C、钠与水反应:Na+H2O=Na++OH-+H2 |
| D、过量二氧化碳通入漂白粉的溶液中 CO2+H2O+ClO-═HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应平衡常数的值为1 |
| B、将容器体积变为20L,Z的平衡浓度减小为0.025mol/L |
| C、以X浓度变化表示的反应速率为0.005mol/(L?s) |
| D、当X、Y、Z的浓度相等时,证明反应达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com