


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
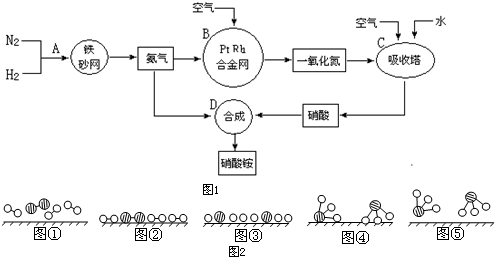
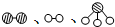 分别表示N2、H2、NH3.
分别表示N2、H2、NH3.
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
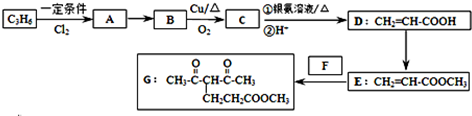
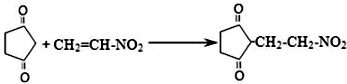
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与NaClO溶液混合后,溶液中c(OH-)/c(H+)变大 |
| B、加入CaCO3粉末后,溶液中c(HClO)变大 |
| C、久置后,溶液中离子种类减少 |
| D、该溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
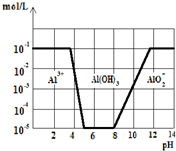 常温下,在0.1mol?L-1KAl(SO4)2溶液中,加入KOH固体,如图,横坐标
常温下,在0.1mol?L-1KAl(SO4)2溶液中,加入KOH固体,如图,横坐标| A、从图中数据计算可得Al(OH)3的溶度积Ksp=10-23 |
| B、沉淀Al3+可以控制溶液pH的范围为5~8 |
| C、向KAl(SO4)2溶液中加入KOH固体至pH=7时,c(K+):c(SO42-)=2:1 |
| D、往KAl(SO4)2溶液中加入足量的氢氧化钾溶液,反应的离子方程式可表示为:Al3++4OH-=AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
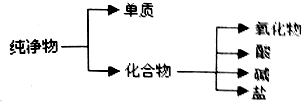 纯净物根据其组成和性质可进行如图所示分类
纯净物根据其组成和性质可进行如图所示分类| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢管与电源正极连接,可对钢管进行电化学保护 |
| B、利用高压氧舱治疗煤气中毒是依据平衡移动原理 |
| C、配制氯化亚锡(SnCl2)溶液时需加适量盐酸防止被氧化变浑浊 |
| D、用Fe除去溶液中的Cu2+、Hg2+与用FeS除去溶液中的Cu2+、Hg2+的原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com