
| A. | (NH4+)2S | B. | Al2(SO4)3 | C. | KOH | D. | HNO3 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,部分碱、大多数盐、金属氧化物、铵盐中都含有离子键,据此分析解答.
解答 解:A.(NH4)2S中铵根离子和硫离子之间存在离子键,为离子化合物,故A不选;
B.Al2(SO4)3中硫酸根离子和铝离子之间存在离子键,为离子化合物,故B不选;
C.KOH是强碱,钾离子和氢氧根离子之间存在离子键,为离子化合物,故C不选;
D.HNO3属于酸,HNO3溶于水也能电离出H+和硝酸根离子,但HNO3是共价化合物,分子中不含离子键,只含共价键,故D选;
故选D.
点评 本题考查离子键的判断,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,注意铵盐中含有离子键,为易错点.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:选择题
| A. | FeO+CO═Fe+CO2 △H=-11kJ•mol-1 | |
| B. | FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-22kJ•mol-1 | |
| C. | FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ•mol-1 | |
| D. | FeO(s)+CO(g)═Fe(s)+CO2(g))△H=11kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 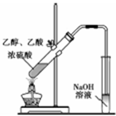 用如图装置制备纯净的乙酸乙酯 | |
| B. | 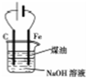 用如图装置制备Fe(OH)2,并能保持一段时间的白色 | |
| C. | 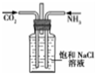 用如图装置先通CO2、在通NH3制备Na2CO3 | |
| D. | 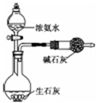 用如图装置制取少量NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>④>②>① | B. | ④>③>②>① | C. | ①>④=③>② | D. | ③=④>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
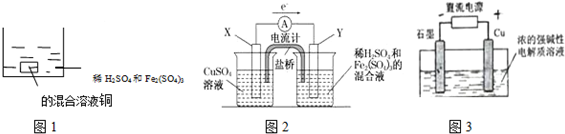
| A. | 如图1 所示将一定量的铜片加入到100 mL 稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO42-)为0.5mol/L | |
| B. | 如图2 所示的装置中发生Cu+2Fe3+═Cu2++2Fe2+的反应,X 极是负极,Y 极的材料名称可以是铜 | |
| C. | Cu2O 是一种半导体材料,基于绿色化学理念设计的制取.Cu2O 的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应 | |
| D. | 如图3 所示当有0.1mol 电子转移时,有0.1molCu2O 生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3+H2O=H2SO4 | B. | CH2=CH2+HClO→CH3-CHOH | ||
| C. | CH3Cl+Cl2→CH2Cl2+HCl | D. | CO2+2NaOH=Na2CO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 金属(粉末状)(mol) | 酸的浓度及体积 | 反应温度(℃) |
| A | Mg,0.1 | 6mol•L-1硝酸10mL | 60 |
| B | Mg,0.1 | 3mol•L-1盐酸10mL | 60 |
| C | Fe,0.1 | 3mol•L-1盐酸100mL | 60 |
| D | Mg,0.1 | 3mol•L-1硫酸5mL | 60 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com