
【题目】Ⅰ.将等质量的锌片和铜片用导线相连插入500 mL CuSO4溶液中构成如图所示的装置。
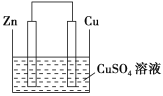
(1)该装置为____装置,该装置中发生反应的总离子方程式为____,铜片周围溶液会出现________的现象。
(2)若2 min后测得锌片的质量减少1.3 g,则导线中流过的电子为_____mol。
(3)若该装置的电解质溶液换为FeCl3溶液,其正极反应为_______。
Ⅱ.向2L密闭容器中通入amol气体A和b mol气体B,在一定条件下发生反应xA(g)+yB(g)![]() pC(g)+qD(g)。已知:平均反应速率v(C)=
pC(g)+qD(g)。已知:平均反应速率v(C)=![]() v(A);反应至2min时,A的物质的量减少了
v(A);反应至2min时,A的物质的量减少了![]() ,B的浓度减少了
,B的浓度减少了![]() amol/L,同时有amolD生成。
amol/L,同时有amolD生成。
(4)0~2 min内,v(A)=__________。
(5)该化学方程式中,y=__________。
(6)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率____(填“增大”、“减小”或“不变”),理由是_____。
【答案】原电池 Zn+Cu2+=Zn2++Cu 颜色变浅 0.04 Fe3++e-=Fe2+ ![]() amol/(L·min) 3 增大 体积减小,反应物的浓度增大,则反应速率增大
amol/(L·min) 3 增大 体积减小,反应物的浓度增大,则反应速率增大
【解析】
I.(1)装置是否有外加电源可以判断所属的类别,根据电池的工作原理来分析电极附近的现象;
(2)根据电极反应式来计算;
(3)电池中的电解质溶液换为FeCl3溶液时,电池反应为Zn+2Fe3+=Zn2++2Fe2+。
II.(4)根据反应速率的概念计算;
(5)速率之比等于化学计量数之比,物质的量之比等于化学计量数之比;
(6)如果其他条件不变,将容器的容积变为1L,进行同样的实验,体积减小,反应物的浓度增大,因而使反应速率增大。
I.(1)装置没有外加电源,有活动性不同的电极、电解质溶液、形成了闭合回路,属于原电池,活泼金属锌作负极,本身失电子,发生反应:Zn-2e-=Zn2+,正极上是Cu2+得电子,正极的电极反应式为Cu2++2e-=Cu,所以Cu2+在该极附近溶度减小,溶液的蓝色变浅,正极反应和负极反应合并即为总的电池反应Zn+Cu2+= Zn2++Cu;
(2)锌极发生的反应为:Zn-2e-=Zn2+,锌片质量减少1.3g,反应的Zn的物质的量为n(Zn)=1.3g÷65g/mol=0.02mol时,由于Zn是+2价的金属,所以反应过程中转移电子物质的量为0.04mol。
(3)若该装置的电解质溶液换为FeCl3溶液,根据总反应:Zn+2Fe3+=Zn2++2Fe2+,可知正极发生还原反应的电极反应式为Fe3++e-=Fe2+;
II.(4)反应2min 时,A的物质的量减少了![]() ,则△c(A)=
,则△c(A)=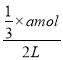 =
=![]() mol/L,0~2min内,v(A)=
mol/L,0~2min内,v(A)=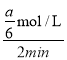 =
=![]() mol/(L·min);
mol/(L·min);
(5)平均反应速率v(C)=![]() v(A),则x:p=2:1,A的物质的量减少了
v(A),则x:p=2:1,A的物质的量减少了![]() ,则消耗的A为
,则消耗的A为![]() ,B的物质的量减少了
,B的物质的量减少了![]() ,有a mol D生成,则x:y:q=
,有a mol D生成,则x:y:q=![]() mol:
mol:![]() mol:amol=2:3:6,所以x:y:p:q=2:3:1:6,因此反应方程式为:2A(g)+3B(g)═1C(g)+6D(g),y=3;
mol:amol=2:3:6,所以x:y:p:q=2:3:1:6,因此反应方程式为:2A(g)+3B(g)═1C(g)+6D(g),y=3;
(6)如果其他条件不变,将容器的容积变为1L,进行同样的实验,体积减小,反应物的浓度增大,因而使反应速率增大。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】已知CH3![]() COOH被还原剂直接还原生成两种乳酸(CH3
COOH被还原剂直接还原生成两种乳酸(CH3![]() COOH)。如果将CH3
COOH)。如果将CH3![]() COOH与薄荷醇(C10H19OH)酯化后,再通过还原反应、水解反应,则得到的主要产物是一种乳酸,实现了不对称合成。其过程如下:
COOH与薄荷醇(C10H19OH)酯化后,再通过还原反应、水解反应,则得到的主要产物是一种乳酸,实现了不对称合成。其过程如下:
CH3COCOOH![]() A
A![]() B
B![]() CH3
CH3![]() COOH
COOH
(1)CH3![]() COOH中________(填“有”或“无”)手性碳原子。CH3
COOH中________(填“有”或“无”)手性碳原子。CH3![]() COOH中___________(填“有”或“无”)手性碳原子,两种乳酸的关系为______________。
COOH中___________(填“有”或“无”)手性碳原子,两种乳酸的关系为______________。
(2)A的分子式为____________,B的分子式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol.试回答:
(1)烃A的分子式为__________.
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则燃烧时消耗标准状况下的氧气____________L.
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为_____________.
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式有三种,它们分别为________、________、_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O==HClO+HSO3-
B. 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合: Al3++2SO42-+2Ba2++4OH- =2BaSO4+AlO2-+ 2H2O
C. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
D. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H+ +2I-=2Fe2+ +I2 +3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
乙:![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)蒸馏过程中温度应控制在80℃~90℃,温度过高或过低都不利于生产,原因是_______。
(2)甲同学步骤④所发生反应的离子方程式为_______。
(3)某同学在进行蒸馏操作时,采用如图所示装置:
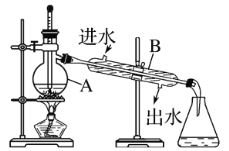
①仪器A的名称是_____
②写出图中两处明显的错误:________。
③实验时A中除加入混合溶液外,还需加入少量_____,其作用是___。
(4)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是____(填“甲”或“乙”),理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硫和钒的相关化合物,在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒的原子结构示意图为____________________________;
(2)VO43-的中心原子价层孤电子对数目为______,一个VO43-离子中含有_______个σ键;
(3)2-巯基烟酸氧钒配合物(图1) 是副作用小的有效调节血糖的新型药物。
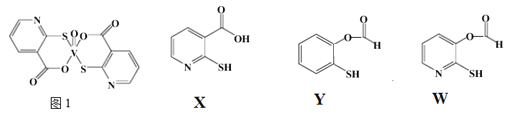
①该药物中N原子的杂化方式是_______;
②X、Y、W三种物质在水中的溶解性由大到小的顺序为________,原因是__________;
已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”(或大π键)。大π键可用![]()
![]() 表示,其中m、n分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中m、n分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为![]()
![]() 。
。
③下列微粒中存在“离域Π键”的是_____;
A.O3 B.SO42- C.H2S D.NO3-
④CS2分子中大π键可以表示为_______________;
(4)偏钒酸铵加热分解生成五氧化二钒、氨气、水。偏钒酸铵的阴离子呈如下图2所示的无限链状结构,则偏钒酸铵的化学式为_________;
(5)某六方硫钒化合物晶体的晶胞如图4所示(![]() 表示V,
表示V,![]() 表示S),该晶胞的化学式为VS。图3 为该晶胞的俯视图。
表示S),该晶胞的化学式为VS。图3 为该晶胞的俯视图。
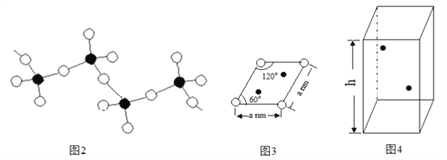
①请在图4中用![]() 标出V原子的位置;
标出V原子的位置;
②已知晶胞的密度为dg/cm3 ,计算晶胞参数h =_____________cm。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
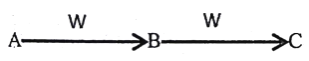
(1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①向B溶液中通入W生成C的离子方程式为__________________________________。
②A溶液与C溶液反应的化学方程式为______________________________________。
(2)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_____________。
②A溶液一步转化为C溶液的反应离子方程式为________________________________。
(3)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1。
①B的化学式为________________。
②实验室制取B时,_____________(填“能”或“不能”)用向上排空气法收集B。
③一定条件下B与CO反应的化学方程式为_____________________________。
(4)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。则C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的含氧衍生物可以作为无铅汽油的抗爆震剂,它的相对分子质量不超过100,含C的质量分数为68.2%,含H的质量分数为13.6%,其余为氧。请计算回答:
(1)该化合物的相对分子质量是____________________。
(2)写出该化合物的分子式___________________________。
(3)若该化合物不能与钠反应产生氢气,红外光谱和核磁共振氢谱显示该分子中有4个甲基。请写出其结构简式。_________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com