
【题目】无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:
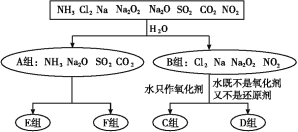
(1)上述分类中,分成A、B两组的依据是_________。
(2)D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有__(填化学式)。
(3)实验室由Al3+制备Al(OH)3时,应选择F组中_____(填化学式)的水溶液,离子方程式为______。
(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___,②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__。
【答案】化合价是否发生变化 Cl2、Na2O2 NH3 Al3+ + 3NH3·H2O == Al(OH)3↓+ 3NH4+ 3NF3 + 5H2O == 2NO + 9HF + HNO3 有红棕色气体生成
【解析】
根据化合价分析可以知道分类是按照化合价是否发生变化来分类,按题给信息来写方程式。
⑴上述分类中,A类是非氧化还原反应,B类是氧化还原反应,因此分成A、B两组的依据是是否有化合价发生变化,
故答案化合价是否发生变化;
⑵D组物质与水反应中,
氯气和水反应生成盐酸和次氯酸,水既不是氧化剂也不是还原剂,氧化剂和还原之比为1:1;
钠和水反应生成氢氧化钠和氢气,水是氧化剂,钠是还原剂,氧化剂和还原剂之比为1:1;
过氧化钠与水反应生成氢氧化钠和氧气,水既不是氧化剂也不是还原剂,氧化剂和还原剂之比为1:1;
二氧化氮和水反应生成硝酸和一氧化氮,水既不是氧化剂也不是还原剂,氧化剂和还原剂之比为1:2;因此D中氯气、过氧化钠氧化剂和还原物质的量之比为1:1;
故答案为Cl2、Na2O2;
⑶实验室由Al3+制备Al(OH)3时,用铝盐和氨水反应,因此应选择F组中NH3的水溶液,离子方程式为 Al3+ + 3NH3·H2O == Al(OH)3↓+ 3NH4+,
故答案为NH3;Al3+ + 3NH3·H2O == Al(OH)3↓+ 3NH4+;
⑷①三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,该反应的化学方程式3NF3 + 5H2O == 2NO + 9HF + HNO3;
故答案为3NF3 + 5H2O == 2NO + 9HF + HNO3;
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,在空气中反应生成的NO与空气中的氧气反应生成红棕色的二氧化氮,因此该气体泄漏时的现象是有红棕色气体生成;
故答案为有红棕色气体生成。


科目:高中化学 来源: 题型:
【题目】一种新型漂白剂(结构如图)可用于漂白羊毛、草等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
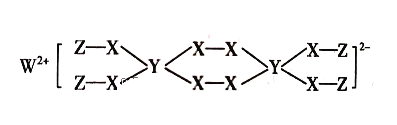
A.元素电负性顺序为:X>W>Y
B.Y的最高价氧化物对应水化物为强酸
C.工业上通过电解熔融的WX来制得W
D.该漂白剂中X、Y均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
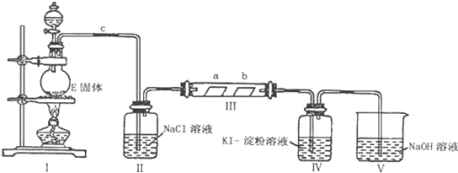
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___。
(2)装置Ⅱ的作用是___。
(3)实验过程中,装置IV中的实验现象为___;发生反应的化学方程式为___。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___装置(填序号),该装置的作用是___。
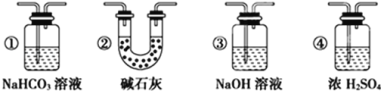
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种线性高分子,结构如下图所示。
![]()
下列有关说法正确的是( )
A. 该高分子由4种单体缩聚而成
B. 构成该高分子的单体中有2种羧酸
C. 上述单体中的乙二醇,可被O2催化氧化生成单体之一的草酸
D. 该高分子有固定熔、沸点,1 mol上述链节完全水解需要氢氧化钠物质的量为 5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用序号填空:
①13C与14C ②正丁烷与异丁烷
③CH3CH3与CH3CH2CH3 ④
(1)属于同位素的是______;
(2)属于同系物的是______;
(3)属于同分异构体的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J均代表无机物或其水溶液,其中A是红色固体,H是生活中常见的液体,J是磁性材料,而B、D、G是单质,B是地壳中含量最高的金属元素,G是气体。根据图示回答问题:
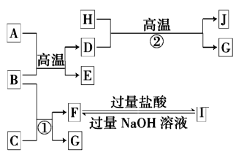
(1)写出下列物质的化学式:A_______,I___________。
(2)反应②的化学方程式是____________。
(3)上述物质D可与硫酸反应生成FeSO4,利用FeSO4可制得一种高效净水剂。方程式如下,若FeSO4和O2的化学计量数之比为2∶1,试配平下列方程式______:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑。
(4)高铁酸钾(K2FeO4)作为高效的绿色水处理剂,在水中发生反应生成Fe(OH)3,高铁酸钾作为水处理剂发挥的作用是____、____。
(5)氧化铁是重要工业颜料,用废铁屑制备氧化铁的流程如下:回答下列问题:
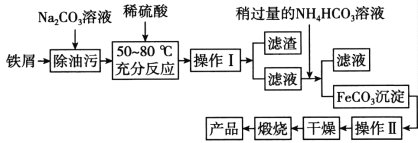
①操作I、Ⅱ的名称分别是_____、_________。
②加入NH4HCO3溶液后过滤,所得滤液的主要成份是:_________。
③写出在空气中锻烧FeCO3的化学方程式________;
(6)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定:a.称取2.850g绿矾 (FeSO4·7H2O)产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为 20.00mL。计算上述样品中FeSO4·7H2O的质量分数为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变化如图。
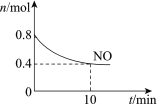
(1)将NO、CO转化为2种无毒气体的化学方程式是______。
(2)反应开始至10 min,v(NO)=______mol/(Lmin)。
(3)下列说法正确的是______。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。该有机物的分子式为______。
Ⅱ.为了证明溴乙烷中存在溴原子,某同学设计如下实验:
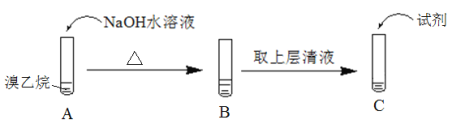
①将试管C中加入的试剂及相应的实验现象补充完整:_________。
②溴乙烷在NaOH水溶液中反应的化学方程式是_____________。
Ⅲ.为实现以下各步转化,请在下列括号中填入适当试剂。______、______
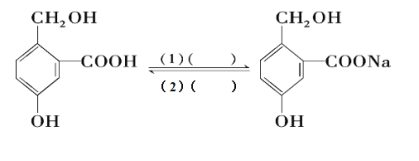
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时某气态烃与O2混合充入密闭容器中,点燃后又恢复至25℃,此时容器内压强为原来的![]() ,再经NaOH溶液处理,容器内几乎成为真空,该烃的化学式为( )
,再经NaOH溶液处理,容器内几乎成为真空,该烃的化学式为( )
A.CH4B.C2H6C.C3H8D.C4H10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com