
【题目】(1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式_________________________________。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
乙:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
①CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________(填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
553 | Cu/ZnO纳米片材料 | 12.0 | 70.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________(填字母符号)。
(3)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
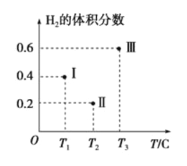
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________。
②三个容器中一定达到平衡状态的是容器________(填写容器代号)。
【答案】8CO2(g)+25H2(g)=C8H18(1)+16H2O(1) ΔH=—(25a-b)KJ/mol K=![]() 小于 降低温度、减小产物浓度 B 0.0875mol/(L·min) Ⅲ
小于 降低温度、减小产物浓度 B 0.0875mol/(L·min) Ⅲ
【解析】
(1)已知:①H2(g)+1/2O2(g)=H2O(l) ΔH1 =—aKJ/mol;
②C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2=—bKJ/mol
根据盖斯定律,由①×25-②得反应方程式:8CO2(g)+25H2(g)=C8H18(1) +16H2O(1) ΔH=25ΔH1-ΔH2=ΔH=—(25a-b)KJ/mol;
(2) ①已知甲:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-53.7 kJ·mol-1平衡常数K1
CH3OH(g)+H2O(g)△H=-53.7 kJ·mol-1平衡常数K1
乙:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H=+41.2 kJ·mol-1平衡常数K2;根据盖斯定律,由甲-乙得反应CO(g)+2H2(g)
CO(g)+H2O(g)△H=+41.2 kJ·mol-1平衡常数K2;根据盖斯定律,由甲-乙得反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=![]() ;△H=-53.7 kJ·mol-1-41.2 kJ·mol-1=-94.9 kJ·mol-1<0;②反应CO(g)+2H2(g)
;△H=-53.7 kJ·mol-1-41.2 kJ·mol-1=-94.9 kJ·mol-1<0;②反应CO(g)+2H2(g) ![]() CH3OH(g)是气体体积缩小的放热反应,提高CO2转化为CH3OH平衡转化率的措施有降低温度、减少产物浓度、按比例充入原料CO2和H2等;③由表中数据分析在相同温度下不同催化剂对甲醇的选择性有显著影响,使用Cu/ZnO纳米片催化剂时甲醇选择性高;使用相同的催化剂在不同温度下,虽然二氧化碳的转化率增加,甲醇的选择性却减小,说明温度升高,副产物增加,因此综合考虑选B选项;
CH3OH(g)是气体体积缩小的放热反应,提高CO2转化为CH3OH平衡转化率的措施有降低温度、减少产物浓度、按比例充入原料CO2和H2等;③由表中数据分析在相同温度下不同催化剂对甲醇的选择性有显著影响,使用Cu/ZnO纳米片催化剂时甲醇选择性高;使用相同的催化剂在不同温度下,虽然二氧化碳的转化率增加,甲醇的选择性却减小,说明温度升高,副产物增加,因此综合考虑选B选项;
(3) ①CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
开始时的物质的量:1 2 0
转化的物质的量: a 2a a
平衡时的物质的量:1-a 2-2a a
容器Ⅱ中0~5 min内H2含量是20%,a=![]() ,v(CH3OH)= 0.0875mol/(L·min);②Ⅲ中温度高氢气含量高,说明达到平衡升高温度平衡逆向移动,氢气含量增加。
,v(CH3OH)= 0.0875mol/(L·min);②Ⅲ中温度高氢气含量高,说明达到平衡升高温度平衡逆向移动,氢气含量增加。


科目:高中化学 来源: 题型:
【题目】已知反应①CO(g)+CuO(s)![]() CO2(g)+Cu(s)和反应②H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②H2(g)+CuO(s)![]() Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A. 反应①的平衡常数K1=c(CO2).c(Cu)/c(CO).c(CuO)
B. 反应③的平衡常数K=K1/K2
C. 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D. 对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律的表述正确的是( )
A.原子序数为15的元素的最高化合价为+3
B.ⅦA族元素是同周期中非金属性最强的元素
C.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
D.I A族元素的金属性一定比ⅡA族元素的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是

A. 该氨水的浓度为0.100 0 mol·L-1
B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-)
C. 点②溶液中c(NH4+)=c(Cl-)
D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
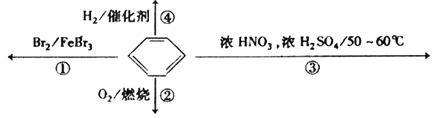
A. 反应![]() 为取代反应,有机产物的密度比水小
为取代反应,有机产物的密度比水小
B. 反应![]() 为取代反应,有机产物是一种烃
为取代反应,有机产物是一种烃
C. 反应![]() 中1mol苯最多与
中1mol苯最多与![]() 发生加成反应,是因为苯分子含有三个碳碳双键
发生加成反应,是因为苯分子含有三个碳碳双键
D. 反应![]() 为氧化反应,反应现象是火焰明亮并带有较多的黑烟
为氧化反应,反应现象是火焰明亮并带有较多的黑烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。工业上,利用乙烯水化法制乙醇:CH2=CH2+H2O![]() CH3CH2OH。下列有关说法正确的是
CH3CH2OH。下列有关说法正确的是
A. 1mol乙烯和1mol乙醇分别完全燃烧,消耗O2的分子数均为3NA
B. 1mol H2O和H2F+的混合物中所含质子数为10NA
C. 乙醇催化氧化生成1mol乙醛时转移电子数为NA
D. 46g乙醇中所含共价键的数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1mL1.00mol·L-1HCl溶液和V2mL未如浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )

A. 做该实验时环境温度为22℃ B. 该实验表明化学能可以转化为热能
C. NaOH溶液的浓度约为1.00mol·L-1 D. 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com