
³£ĪĀĻĀ£¬Ļņ20mL0.2mol/LH2AČÜŅŗÖŠµĪ¼Ó0.2mol/LNaOHČÜŅŗ”£ÓŠ¹ŲĪ¢Į£µÄĪļÖŹµÄĮæ±ä»ÆČēĻĀĶ¼£ØĘäÖŠ¢ń“ś±ķH2A£¬¢ņ“ś±ķHA-£¬¢ó“ś±ķA2-£©øł¾ŻĻĀĶ¼Ķ¼Ź¾ÅŠ¶Ļ£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©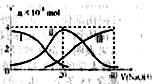
A£®µ±V£ØNaOH£©=20mLŹ±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµ£ŗc(Na+)>c(HA”„£©>c(H+)> c(A2£)>c(OH”„)
B£®µČĢå»żµČÅØ¶ČµÄNaOHČÜŅŗÓėH2AČÜŅŗ»ģŗĻŗó£¬ĘäČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č±Č“æĖ®µÄ“ó
C£®NaHAČÜŅŗÖŠ£ŗc(OH-)£«c(A2ØC)£½c(H+)£«c(H2A)
D£®ĻņNa2AČÜŅŗ¼ÓČėĖ®µÄ¹ż³ĢÖŠ£¬pH¼õŠ”
B
½āĪöŹŌĢā·ÖĪö£ŗA£®µ±V£ØNaOH£©="20" mLŹ±£¬·¢Éś·“Ó¦ĪŖNaOH+H2A=NaHA+H2O£¬ČÜŅŗÖ÷ŅŖĪŖNaHA£¬ÓÉĶ¼æÉÖŖc£ØA2-£©£¾c£ØH2A£©£¬ĖµĆ÷HA-µēĄė“óÓŚĖ®½ā³Ģ¶Č£¬ČÜŅŗĻŌĖįŠŌ£¬Ōņc£ØNa+£©£¾c£ØHA-£©£¾c£ØH+£©£¾c£ØA2-£©£¾c£ØOH-£©£¬ÕżČ·£»B£®ÓÉĶ¼Ź¾¹ŲĻµÖŖ£¬c£ØA2-£©£¾c£ØH2A£©£¬ĖµĆ÷µēĄė“óÓŚĖ®½ā³Ģ¶Č£¬ČÜŅŗĻŌĖįŠŌ£¬Ė®µÄµēĄėŹÜµ½ĮĖŅÖÖĘ£¬“ķĪó£»C£®øł¾ŻµēŗÉŹŲŗćµĆc£ØOH-£©+2c£ØA2-£©+c£ØHA-£©=c£ØH+£©+c£ØNa+£©£¬øł¾ŻĪļĮĻŹŲŗćµĆc£ØNa+£©=c£ØHA-£©+c£ØH2A£©+c£ØA2-£©£¬ĖłŅŌµĆc£ØOH-£©+c£ØA2-£©=c£ØH+£©+c£ØH2A£©£¬ÕżČ·£»D£®Na2AČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬“Ł½ųĘäĖ®½ā£¬µ«ČÜŅŗÖŠĒāŃõøłĄė×ÓÅØ¶Č¼õŠ”£¬ĖłŅŌČÜŅŗµÄpH¼õŠ”£¬ÕżČ·£¬“š°øŃ”B”£
æ¼µć£ŗæ¼²éĖį¼ī»ģŗĻ¼ĘĖć£¬Ąė×ÓÅØ¶ČµÄ“óŠ”±Č½Ļ£¬ŃĪµÄĖ®½āµÄÓ¦ÓĆ£¬Ė®µÄµēĄė£¬ŹŲŗć¹ęĀɵÄÓ¦ÓĆ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
»ÆѧÓėÉē»į”¢Éś»īĆÜĒŠĻą¹Ų”£¶ŌĻĀĮŠĻÖĻó»ņŹĀŹµµÄ½āŹĶÕżČ·µÄŹĒ
| Ń”Ļī | ĻÖĻó»ņŹĀŹµ | ½āŹĶ |
| A | ÓĆČȵÄÉÕ¼īČÜŅŗĻ“Č„ÓĶĪŪ | Na2CO3æÉÖ±½ÓŗĶÓĶĪŪ·“Ó¦ |
| B | ĘÆ°×·ŪŌŚæÕĘųÖŠ¾ĆÖƱäÖŹ | ĘÆ°×·ŪÖŠµÄCaCl2 ÓėæÕĘųÖŠµÄCO2·“Ӧɜ³ÉCaCO3 |
| C | Ź©·ŹŹ±£¬²ŻÄ¾»Ņ(ÓŠŠ§³É·ÖĪŖK2CO3)²»ÄÜÓėNH4Cl»ģŗĻŹ¹ÓĆ | K2CO3ÓėNH4Cl·“Ӧɜ³É°±Ęų»į½µµĶ·ŹŠ§ |
| D | FeCl3ČÜŅŗæÉÓĆÓŚĶÖŹÓ”Ė¢ĻßĀ·°åÖĘ×÷ | FeCl3ÄÜ“Óŗ¬ÓŠCu2£«µÄČÜŅŗÖŠÖĆ»»³öĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŹŅĪĀĻĀ£¬½«Ņ»ŌŖĖįHAµÄČÜŅŗŗĶKOHČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌĢå»ż±ä»Æ£©£¬ŹµŃ鏿¾ŻČēĻĀ±ķ£ŗ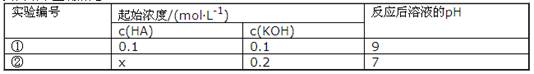
ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ£Ø £©
A£®ŹµŃé¢Ł·“Ó¦ŗóµÄČÜŅŗÖŠ£ŗc£ØK+£©>c£ØA££©>c£ØOH££©>c£ØH+£©
B£®ŹµŃé¢Ł·“Ó¦ŗóČÜŅŗÖŠ£ŗc£ØOH££©=c£ØK+£©£c£ØA££©=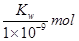 ”¤L£1
”¤L£1
C£®ŹµŃé¢Ś·“Ó¦ŗóµÄČÜŅŗÖŠ£ŗc£ØA££©+c£ØHA£©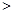 0£®1mol”¤L-l
0£®1mol”¤L-l
D£®ŹµŃé¢Ś·“Ó¦ŗóµÄČÜŅŗÖŠ£ŗc£ØK+£©=c£ØA££©>c£ØOH££©=c£ØH+£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ij»Æѧъ¾æŠŌѧĻ°Š”×é¶Ōµē½āÖŹČÜŅŗ×÷ČēĻĀµÄ¹éÄÉ×ܽį£Ø¾łŌŚ³£ĪĀĻĀ£©£¬ĘäÖŠÕżČ·µÄŹĒ
¢Ł pH£½1µÄĒæĖįČÜŅŗ£¬¼ÓĖ®Ļ”ŹĶŗó£¬ČÜŅŗÖŠø÷Ąė×ÓÅØ¶Č¶¼»į½µµĶ
¢Ś 1 L 0.50 mol”¤L£1NH4Cl ČÜŅŗÓė2 L 0.25 mol”¤L£1NH4Cl ČÜŅŗŗ¬NH4+ ĪļÖŹµÄĮæĶźČ«ĻąµČ
¢Ū pHĻąµČµÄĖÄÖÖČÜŅŗ£ŗa£®CH3COONa b£®C6H5ONa c£®NaHCO3 d£®NaOH£¬ŌņĖÄÖÖČÜŅŗµÄČÜÖŹµÄĪļÖŹµÄĮæÅضČÓÉŠ”µ½“óĖ³ŠņĪŖ£ŗd < b < c < a
¢Ü pH=8.3µÄNaHCO3ČÜŅŗ£ŗc(Na£«) £¾ c(HCO3£) £¾ c(CO32£)£¾ c(H2CO3)
¢Ż pH£½2µÄŅ»ŌŖĖįŗĶpH£½12µÄ¶žŌŖĒæ¼īµČĢå»ż»ģŗĻ£ŗc(OH£) ”Ü c(H£«)
¢ŽpH£½4”¢ÅØ¶Č¾łĪŖ0.1mol”¤L£1µÄCH3COOH”¢CH3COONa»ģŗĻČÜŅŗÖŠ£ŗc(CH3COO£)£«c(OH£) £¾ c(CH3COOH)£«c(H+)
| A£®¢Ł¢Ś¢Ü | B£®¢Ł¢Ū¢Ż | C£®¢Ū¢Ż¢Ž | D£®¢Ś¢Ü¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬½«Ä³Ņ»ŌŖĖįHAŗĶNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬Į½ÖÖČÜŅŗµÄÅضČŗĶ»ģĢØŗóĖłµĆČÜŅŗ
µÄpHČēĻĀ±ķ£ŗ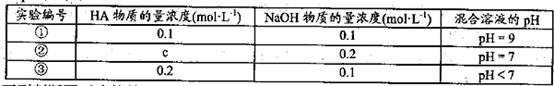
ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ
A£®HAµÄµēĄė·½³ĢŹ½ĪŖ£ŗ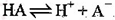 |
B£®²»æ¼ĀĒĘäĖū×éµÄŹµŃé½į¹ū£¬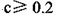 |
C£®¢Ū×鏵ŃéÖŠ£¬»ģŗĻČÜŅŗÖŠ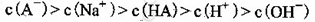 |
D£®¢Ł×鏵ŃéÖŠ£¬»ģŗĻČÜŅŗÖŠ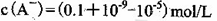 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠČÜŅŗÖŠµÄĮ£×ÓÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ
| A£®0.1 mol/L NaHCO3ČÜŅŗÖŠ£ŗc(Na+)£¾c(HCO3-)£¾c(CO32-)£¾c(H2CO3) |
| B£®1L0.1 mol/L Na2SČÜŅŗÖŠ£ŗc(OH-)-c(H+)£½c(HS-)+c(H2S) |
| C£®ŹŅĪĀĻĀ£¬pH£½3.5µÄøĢéŁÖÖŠc(H+)ŹĒpH£½6.5µÄÅ£ÄĢÖŠc(H+)µÄ1000±¶ |
| D£®µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄNaXŗĶČõĖįHX»ģŗĻŗóµÄČÜŅŗÖŠ£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®Į½ÖÖÄŃČÜĪļÖŠČܽā¶ČŠ”µÄĪļÖŹĘäKSP²»Ņ»¶ØŠ” |
| B£®Ķ¬ÖÖĖįŠĪ³ÉµÄĖįŹ½ŃĪČܽā¶ČŅ»¶Ø±ČÕżŃĪµÄČܽā¶Č“ó |
| C£®ŅņĪŖKsp(BaSO4)= 1£®08”Įl0£l0£¬Ksp(BaCO3)=8£®1”Į10£9£¬ĖłŅŌBaSO4³Įµķ²»æÉÄÜ×Ŗ»ÆĪŖBaCO3³Įµķ |
| D£®ĻąĶ¬ĪĀ¶ČĻĀ£¬½«×ćĮæAgCl¹ĢĢå·Ö±š¼ÓČėĶ¬Ģå»żµÄ¢Ł0£®1mo1”¤L£lŃĪĖį”¢¢Ś0£®1mo1”¤L£1ĀČ»ÆĆ¾ČÜŅŗ”¢¢Ū0£®1mo1”¤L£l lĻõĖįŅųČÜŅŗÖŠ£¬c£ØAg+£©£ŗ¢Ū>¢Ś>¢Ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¹ż³Ģ»ņĻÖĻóÓėŃĪĄąĖ®½āĪŽ¹ŲµÄŹĒ
| A£®“æ¼īČÜŅŗČ„ÓĶĪŪ | B£®Ļ”“×ĖįČÜŅŗ¼ÓČČŹ±ĘäpH ¼õŠ” |
| C£®Š”ĖÕ“ņČÜŅŗÓėAlCl3ČÜŅŗ»ģŗĻ²śÉśĘųĢåŗĶ³Įµķ | D£®ÅصÄĮņ»ÆÄĘČÜŅŗÓŠ³ōĪ¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ£ŗ25 ”ꏱ£¬CaCO3µÄKsp=2.8”Į10£9£¬CaCO3ŌŚĖ®ÖŠµÄČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®xŹżÖµĪŖ1.4”Į10£5 |
| B£®bµćÓėdµć¶ŌÓ¦µÄČܶȻżĻąµČ |
| C£®¼ÓČėÕōĮóĖ®æÉŹ¹ČÜŅŗÓÉdµć±äµ½aµć |
| D£®cµć½«ÓŠ³ĮµķÉś³É£¬Ę½ŗāŗóČÜŅŗÖŠc(Ca2+)”¢c(CO32£)Ņ»¶ØĻąµČ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com