
根据FeS2+O2—→Fe2O3+SO2,回答下列问题:
(1)氧化剂________,还原剂________,氧化产物________,还原产物________。
(2)元素化合价升高的元素为________,元素化合价降低的元素为________。
(3)1“分子”还原剂化合价升高总数为________,1“分子”氧化剂化合价降低总数为________。
(4)配平后各物质的系数依次为____________________。
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
下列各离子组能大量共存的是( )
A.Fe3+、NH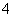 、H+、SO
、H+、SO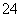
B.Fe3+、Br-、Na+、I-
C.Fe2+、AlO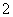 、Na+、NO
、Na+、NO
D.Fe3+、HCO 、NH
、NH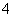 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
柑橘中柠檬烯的结构可表示为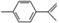 ,下列关于这种物质的说法中正确的是( )
,下列关于这种物质的说法中正确的是( )
A.与苯的结构相似,性质也相似
B.可使溴的四氯化碳溶液褪色
C.易发生取代反应,难发生加成反应
D.该物质极易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有机物结构或性质的描述中错误的是( )
A.将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应
B.苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键
C.乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 mol H2O
D.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬烯是一种食用香料,其结构简式如图所示。
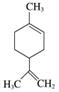
下列有关柠檬烯的分析正确的是( )
A.它的一氯代物有8种
B.它的分子中所有的碳原子一定在同一平面上
C.它和丁基苯(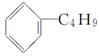 )互为同分异构体
)互为同分异构体
D.一定条件下,它分别可以发生加成、取代、氧化、还原等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
现有24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应。已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为( )
A.+2 B.+3 C.+4 D.+5
查看答案和解析>>
科目:高中化学 来源: 题型:
CuSO4溶液与K2C2O4溶液混合生成一种蓝色钾盐水合物KxCuy(C2O4)z·nH2O。通过下述实验确定该晶体的组成。(已知:MnO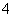 在酸性条件下,加热能分解为O2,同时生成Mn2+。)
在酸性条件下,加热能分解为O2,同时生成Mn2+。)
步骤a:称取0.672 0 g样品,放入锥形瓶,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 mL水加热,用0.200 0 mol·L-1 KMnO4溶液滴定至终点,消耗8.00 mL KMnO4溶液。有关反应:2MnO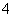 +5C2O
+5C2O +16H+===2Mn2++8H2O+10CO2↑。
+16H+===2Mn2++8H2O+10CO2↑。
步骤b:接着将溶液充分加热。冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI。用0.250 0 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗8.00 mL Na2S2O3溶液。滴定时反应为I2+2S2O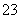 ===2I-+S4O
===2I-+S4O 。
。
(1)步骤b中生成白色沉淀的离子方程式:________________________________________________________________________。
(2)步骤b中“将溶液充分加热”的目的是________________________________________________________________________。
(3)请完成下列确定样品组成的计算过程。
①计算样品中n(C2O )(写出计算过程)
)(写出计算过程)
________________________________________________________________________。
②计算样品中n(Cu2+)(写出计算过程)
________________________________________________________________________。
③根据________原理可求出n(K+),再依据________原理求得n(H2O)。
④该样品晶体的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50 ℃时反应可产生它。下列有关叙述中错误的是( )
A.“某物质”具有还原性
B.CuH与盐酸反应,可能产生H2
C.CuH与足量的稀硝酸反应:CuH+3H++NO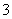 ===Cu2++NO↑+2H2O
===Cu2++NO↑+2H2O
D.CuH在氯气中燃烧:CuH+Cl2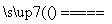 CuCl+HCl
CuCl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、硫的含量影响钢铁性能,碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2。
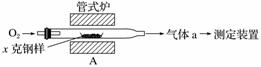
①气体a的成分是________________。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2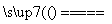
1________+3________。
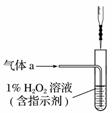
(2)将气体a通入测硫装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式
________________________________________________________________________
________________________________________________________________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液,若消耗1 mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。
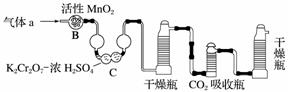
①气体a通过B和C的目的是__________________________________________。
②计算钢样中碳的质量分数,应测量的数据是________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com