
【题目】一种突破传统电池设计理念的镁—锑液态金属储能电池工作原理如下图所示,该电池所用液体密度不同,在重力作用下分为三层,工作时中间层熔融盐的组成及浓度不变。该电池工作一段时间后,可由太阳能电池充电。下列说法不正确的是
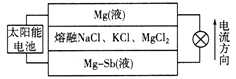
A. 放电时,Mg(液)层的质量减小
B. 放电时正极反应为:Mg2++2e—=Mg
C. 该电池充电时,Mg—Sb(液)层发生还原反应
D. 该电池充电时,C1—向中层和下层分界面处移动
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加罗常数的值,下列说法正确的是( )
A. 常温常压下,2.2gCO2中含有的分子数为0.05NA
B. 0.5molNa2CO3固体中含有的Na+数为0.5NA
C. 32 g O2所含的原子数目为NA
D. 标准状况下,2.24LCCl4含有的碳原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于浓硫酸的性质,下列说法错误的是( )
A.浓硫酸的吸水性和脱水性是一样的B.浓硫酸有酸性和强氧化性
C.浓硫酸有吸水性和脱水性D.浓硫酸能做干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图中表示将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数
B. 实验室用图乙装置滴定FeSO4溶液
C. 实验室用图丙装置脱结晶水得无水硝酸铜固体
D. 图丁表示常温下CaSO4在水中的沉淀溶解平衡曲线,图中a点溶液可通过蒸发变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下表有关铁难溶化合物的溶度积,有关说法正确的是
化合物 | 溶度积(25℃) | 化合物 | 溶度积(25℃) |
FeCO3 | 3.2×10-11 | Fe(OH)3 | 4.0×10-38 |
Fe(OH)2 | 8.0×10-11 | FeS | 6.3×10-18 |
A. 在c(CO32-)=0.1 mol·L-1的溶液中,c(Fe2+)≥3.2×10-10 mol·L-1
B. 将FeCl3和 FeCl2溶液分别调至PH=10,则c(Fe2+)< c(Fe3+)
C. 增加溶液的酸性,有利于将Fe2+沉淀为FeS和FeCO3
D. 将反应液中的Fe2+氧化为 Fe3+有利于将铁从溶液中除尽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于燃料电池的说法正确的是
A.燃料电池是通过燃烧方式将化学能转换为电能
B.氢氧燃料电池中,通入氢气的一极为正极
C.氢氧燃料电池是一种环境友好电池
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的某试剂充分反应,过滤结晶即可;②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶解,再加入适量的氢氧化镁,充分反应,过滤结晶即可;③为了除上硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为_____________(填化学式)而除去。
(2)①中加入的试剂应该选择_____为宜。
(3)②中除去Fe3+所发生的总反应的离子方程式:______________________________。
(4)下列与方案③相关的叙述中,正确的是__________(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.在pH<4 的溶液中Fe3+一定不能大量存在
C.调节溶液pH=4 可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4 的溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,海水中所含食盐高达4×1016t。用海水可生产食盐和金属镁或镁的化合物,其过程如下图所示。
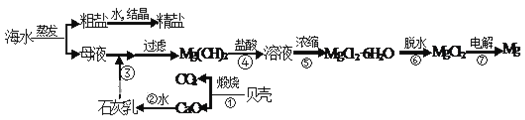
请回答
(1)贝壳主要成分的化学式_________________;
(2)步骤④反应的离子方程式____________________________________________;
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤,
A.粗盐提纯过程中过滤的目的是____________(填序号)
①获得NaCl晶体 ②除去难溶性物质 ③除去易挥发物质 ④除去可溶性物质
B.过滤需要用到的玻璃仪器有玻璃棒______________、______________。
(4)电解MgCl2制金属Mg的反应方程式为MgCl2![]() Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg_______g,同时可得到氯气__________L(标准状况)。
Mg+Cl2↑。电解0.2molMgCl2可生成金属Mg_______g,同时可得到氯气__________L(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com