
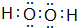 .写出甲的一种用途作高能燃料.
.写出甲的一种用途作高能燃料. 分析 I.(1)Cl2氧化NaClO2溶液制取ClO2,还生成NaCl;
(2)KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,还生成KCl、HCl;
Ⅱ.(1)6.4g甲完全燃烧得到4.48L的氮气(已折算成标准状况),则甲中含有N元素;甲可以与新制Cu(OH)2反应生成砖红色沉淀,砖红色沉淀为Cu2O,同时生成密度为1.25g/L的无色无味的气体,该气体含有N元素,其相对分子质量=1.25×22.4=28,故该气体为N2,由由元素守恒可知,反应还生成水,且甲中还含有H元素,4.48L氮气的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,其质量=0.2mol×28g/mol=5.6g,故6.4g甲中H元素质量=6.4g-5.6g=0.8g,故H原子物质的量=$\frac{0.8g}{1g/mol}$=0.8mol,则甲中N、H原子数目之比=0.2mol×2:0.8mol=1:2,故甲为N2H4;
(2)次氯酸钠与过量氨气反应生成N2H4,根据氧化还原反应可知,还生成NaCl,根据元素守恒可知有水生成;次氯酸钠具有强氧化性,可以氧化N2H4,过量的氨气防止N2H4被氧化;
(3)N2H4与新制Cu(OH)2反应生成氧化亚铜、氮气与水;
(4)乙是一种与甲含有相同电子数的液态物质,它可与甲反应生成一种常见的液态化合物和一种常见的稳定单质,同时放出大量的热,则乙为H2O2.
解答 解:I.(1)Cl2氧化NaClO2溶液制取ClO2,还生成NaCl,离子反应为Cl2+ClO2-=2ClO2+2Cl-,故答案为:Cl2+ClO2-=2ClO2+2Cl-;
(2)KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,还生成KCl、HCl,化学反应方程式为2KMnO4+C2HCl3═2KCl+2CO2↑+2MnO2+HCl,
故答案为:2KMnO4+C2HCl3═2KCl+2CO2↑+2MnO2+HCl;
Ⅱ.(1)6.4g甲完全燃烧得到4.48L的氮气(已折算成标准状况),则甲中含有N元素;甲可以与新制Cu(OH)2反应生成砖红色沉淀,砖红色沉淀为Cu2O,同时生成密度为1.25g/L的无色无味的气体,该气体含有N元素,其相对分子质量=1.25×22.4=28,故该气体为N2,由由元素守恒可知,反应还生成水,且甲中还含有H元素,4.48L氮气的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,其质量=0.2mol×28g/mol=5.6g,故6.4g甲中H元素质量=6.4g-5.6g=0.8g,故H原子物质的量=$\frac{0.8g}{1g/mol}$=0.8mol,则甲中N、H原子数目之比=0.2mol×2:0.8mol=1:2,故甲为N2H4,
故答案为:N2H4;
(2)次氯酸钠与过量氨气反应生成N2H4,根据氧化还原反应可知,还生成NaCl,根据元素守恒可知有水生成,反应方程式为:NaClO+2NH3═N2H4+NaCl+H2O;次氯酸钠具有强氧化性,可以氧化N2H4,过量的氨气防止N2H4被氧化;
故答案为:NaClO+2NH3═N2H4+NaCl+H2O;次氯酸钠具有强氧化性,可以氧化N2H4,过量的氨气防止N2H4被氧化;
(3)N2H4与新制Cu(OH)2反应生成氧化亚铜、氮气与水,反应方程式为:4Cu(OH)2+N2H4═2Cu2O+N2+6H2O,
故答案为:4Cu(OH)2+N2H4═2Cu2O+N2+6H2O;
(4)乙是一种与甲含有相同电子数的液态物质,它可与甲反应生成一种常见的液态化合物和一种常见的稳定单质,同时放出大量的热,则乙为H2O2,其电子式为: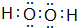 ,N2H4可以作高能燃料,
,N2H4可以作高能燃料,
故答案为: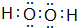 ;作高能燃料.
;作高能燃料.
点评 本题考查无机物推断,为高频考点,属于计算推断型题目,涉及内容在中学中基本没有接触,侧重分析、计算、推断能力的综合考查,注意N、Cl及其化合物的性质及应用,综合性较强,题目难度中等.


科目:高中化学 来源: 题型:选择题
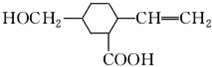 某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )
某有机物的结构如图所示,下列各项性质中,它不可能具有的是( )| A. | ①④ | B. | ⑤ | C. | ④⑥ | D. | ⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3v生成(N2)=v生成(H2) | B. | v消耗(N2)=v消耗(NH3)? | ||
| C. | v消耗(N2)=3v生成(H2)? | D. | 2v消耗(H2)=3v消耗(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数ω=$\frac{A}{(A+V)}×100%$ | |
| B. | 溶质的物质的量浓度c=$\frac{1000ρA}{(MA+MV)}mol•{L}^{-1}$ | |
| C. | 1mL该溶液中n(Cl-)=$\frac{nρAV}{M(A+V)}mol$ | |
| D. | 该温度下此盐的溶解度S=$\frac{100A}{V}g$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com