
| A. | 分子式分别为C2H6和C4H10的两种有机化合物一定互为同系物 | |
| B. | 某反应过程中的能量变化如图所示,可见催化剂能改变该反应的焓变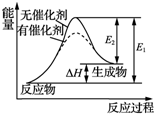 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 1 mol N2与3 mol H2在一定条件下充分反应可得2 mol NH3 |
分析 A.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
B.催化剂能降低活化能;
C.酸性氧化物是能与碱生成盐和水的反应,一般是非金属氧化物;
D.氮气与氢气的反应是可逆反应.
解答 解:A.C2H6和C4H10都为烷烃,结构相似,为同系物,故A正确;
B.催化剂能降低活化能,不改变焓变,故B错误;
C.酸性氧化物是能与碱生成盐和水的反应,一般是非金属金属氧化物,但有些非金属氧化物不一定是酸性氧化物,如一氧化碳等,故C错误;
D.氮气与氢气的反应是可逆反应,不能进行到底,故D错误.
故选A.
点评 本题考查同系物、反应热、物质的分类以及可逆反应等,有利于培养学生的良好的科学素养,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的第一电离能越大,其金属性越强 | |
| B. | 元素的第一电离能越小,其金属性越强 | |
| C. | 金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关 | |
| D. | 同周期元素,第一电离能随原子序数增大逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
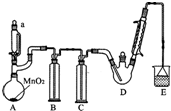 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3$\stackrel{盐酸}{→}$AlCl3(aq)$\stackrel{蒸发}{→}$无水AlCl3 | |
| B. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{Cu}{→}$Fe | |
| C. | NaOH(aq)$\stackrel{CuSO_{4}(aq)}{→}$Cu(OH)2$→_{△}^{葡萄糖}$Cu2O | |
| D. | NH3$→_{催化剂}^{O_{2},△}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
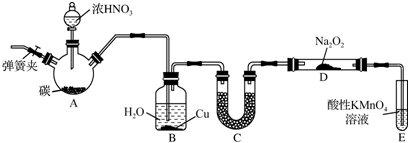
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
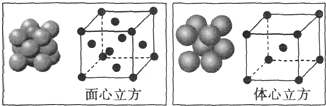 铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:
铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com