
【题目】化学方程式为3MnO2+6KOH+KClO3 ![]() 3K2MnO4+KCl+3H2O,下列说法中正确的( )
3K2MnO4+KCl+3H2O,下列说法中正确的( )
A.反应中MnO2是氧化剂
B.该反应属于复分解反应
C.KClO3在反应中失去电子
D.反应中每生成l mol K2MnO4 , 氧化剂得到2 mol电子
科目:高中化学 来源: 题型:
【题目】25℃,几种物质的pH和浓度如下表所示。
序号 | ① | ② | ③ | ④ |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
pH | 11 | 11 | 3 | 3 |
浓度 | c1 | c2 | c3 | c4 |
回答下列问题:
(1) c1_____(填“>”“<”或“=”) c2。
(2)溶液中水的电离程度②_____(填“>”“<”或“=”)③。
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为________(填序号)。
(4) ①溶液与④溶液等体积混合,溶液的pH_______(填“>"'<"或“=”,下同)7,混合溶液中c(NH4+)____c(Cl-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用粗铜(含杂质Fe)制备氯化铜。
(1)采用如下图所示的装置进行实验(部分仪器和夹持、加热装置已略去)。
①仪器A的名称是________________;
②实验开始前,需要做的操作是____________________。
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为______(填“是”或“否”)必需。原因_______________________________________。
④实验过程中,装置C内的现象是___________________________________。
⑤氢氧化钠溶液的作用是______________________________,其中发生反应的主要离子方程式___________________________、________________________。
(2)若将C中所得固体加稀硫酸溶解。取少量溶液于小试管中,滴加2滴KSCN溶液,无现象。请用必要的文字和离子方程式解释出现这一现象的原因_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=l 的某溶液 A 中除H+外,还含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、 Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol·L-1。现取该溶液进行有关实验,实验结果如下图所示,下列有关说法正确的是

A. 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B. 实物消耗Cu14.4g,则生成气体丁的体积为3.36L
C. 该溶液一定没有Fe3+,但是无法确定是否含有I-
D. 沉淀乙一定有BaCO3,可能有BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关品格能的说法错误的是( )
A.晶格能越大,离子晶体越稳定
B.晶格能越大,离子晶体的硬度越小
C.晶格能越大,离子晶体的能量越低
D.晶格能越大,离子晶体的熔点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列反应回答相应问题.
①3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
未被还原的硝酸与参加反应的总硝酸的质量比为 .
②S+2KNO3+3C ![]() K2S+N2↑+3CO2↑ 还原剂是还原产物是
K2S+N2↑+3CO2↑ 还原剂是还原产物是
③3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是
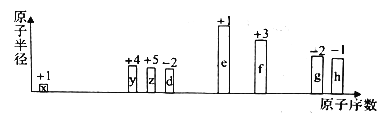
A. 离子半径的大小顺序:d
B. 与x形成简单化合物的沸点:y>z>d
C. 除去实验后试管中残留的g单质,可用热的氢氧化钠溶液
D. g、h的氧化物对应的水化物的酸性:h>g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了验证CH4是否具有还原性,设计了如下实验:
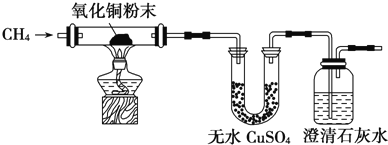
(1)实验过程中观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为________________________________;
(2)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是___________________;请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图)_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com