
在一密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是 ( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能存在的数据是 ( )
A.SO2为0.4 mol·L-1、O2为0.2 mol·L-1
B.SO2为0.25 mol·L-1
C.SO2、SO3均为0.15 mol·L-1
D.SO3为0.4 mol·L-1
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
下列操作或说法正确的是( )
A.乙醇可作为提取碘水中碘的萃取剂
B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C.加入过量浓溴水除去苯中混有的少量苯酚
D.分离乙二醇和丙三醇应采用分液的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
CH3—CHC=H2+HBr→CH3—CHBr—CH3,1 mol某烃A充分燃烧后可以得到8 mol CO2和 4 mol H2O。该烃A在不同条件下能发生如图所示的一系列变化。
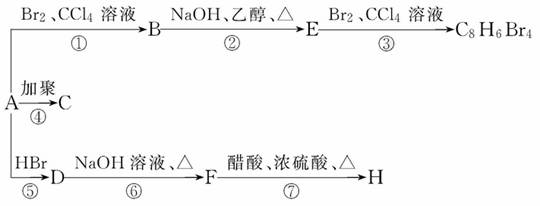
(1)A的化学式:_______________,A的结构简式:_______________________。
(2)上述反应中,①是_________反应,⑦是________反应(填反应类型)。
(3)写出C、D、E、H物质的结构简式:
C_________,D_________,E_________,H_________。
(4)写出D→F反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在容积为10 L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率
4NO(g)+6H2O(g)在容积为10 L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率 (x)(反应物的消耗速率或产物的生成速率)可表示为 ( )
(x)(反应物的消耗速率或产物的生成速率)可表示为 ( )
A. (NH3)=0.010 0 mol·L-1·s-1
(NH3)=0.010 0 mol·L-1·s-1
B. (O2)=0.001 0 mol·L-1·s-1
(O2)=0.001 0 mol·L-1·s-1
C. (NO)=0.001 0 mol·L-1·s-1
(NO)=0.001 0 mol·L-1·s-1
D. (H2O)=0.045 0 mol·L-1·s-1
(H2O)=0.045 0 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是 ( )
A.化学方程式为2M N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
用电解法提取氯化铜废液中的铜,方案正确的是( )
A.用铜片连接电源的正极,另一电极用铂片
B.用碳棒连接电源的正极,另一电极用铜片
C.用氢氧化钠溶液吸收阴极产物
D.用带火星的木条检验阳极产物
查看答案和解析>>
科目:高中化学 来源: 题型:
历史上最早应用的还原性染料是靛蓝,其结构简式为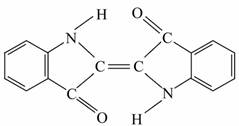 ,下列关于靛蓝的叙述中正确的是( )
,下列关于靛蓝的叙述中正确的是( )
A.它的分子式是C16H10N2O2
B.该物质属于芳香烃
C.该物质含有酯基
D.该物质不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
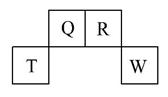 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
(1)T的原子结构示意图为 。
(2)元素的非金属性(原子的得电子能力):
Q W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为__________________________________
__________________________________________________________________。
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是_________________________________________________。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com