
【题目】在溶液中能大量共存,若加入 OH-就有沉淀析出,若加入 H+就能放出气体的是( )
A. Ca2+、 Na+、 Cl-、 SO32- B. Ba2+、 K+、 OH-、 NO3-
C. H+、 Fe3+、 NH4+、 SO42- D. Na+、 Ca2+、 Cl-、 HCO3-
科目:高中化学 来源: 题型:
【题目】(多选)某密闭容器中发生反应:X(g)+Y(g)3Z(g)△H<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( ) 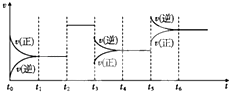
A.t2时加入了催化剂
B.t3时降低了温度
C.t5时增大了压强
D.t4~t5时间内转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列无色溶液中的离子组可以大量共存的是( )
A. K+、Na+、CO32-、SO42- B. K+、Cu2+、Cl-、SO42-
C. Ba2+、H+、NO3-、SO42- D. H+、Ca2+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子能大量共存的一组是: ( )
A. Na+、 Pb2+、 SO42-、 Cl- B. Mg2+、 CO32-、 Cl-、 NO3-
C. Mg2+、 SO42-、 K+、 NH4+ D. Ca2+、 OH-、 Ba2+、 NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应SO2(g)+ ![]() O2(g)SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)2SO2(g)+O2(g)的平衡常数K2的值为( )
O2(g)SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)2SO2(g)+O2(g)的平衡常数K2的值为( )
A.2500
B.100
C.4×10﹣4
D.2×10﹣2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G在催化、药物、新材料等方面有广泛应用.合成G的一种路线如下: 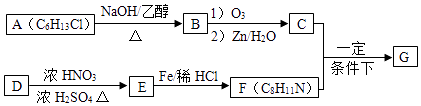
已知以下信息:
① 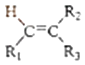
![]() R1CHO+
R1CHO+ 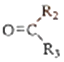
②1mol B经上述反应可生成2mol C,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢原子
⑤RNH2+ 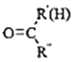
![]()
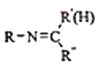 +H2O
+H2O
回答下列问题:
(1)C中官能团名称 , D的化学名称 .
(2)由A生成B的化学方程式为 .
(3)G的结构简式为 .
(4)F的同分异构体中含有苯环的还有种(不考虑立体异构),其中核磁共振氢谱有4组峰,且面积比为6:2:2:1的是(写出其中一种的结构简式).
(5)由苯及化合物C经如下步骤可合成N﹣异丙基苯胺: ![]()
![]() H
H ![]() I
I ![]() J
J ![]()
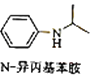
反应条件1所选择的试剂为 , H→I的反应类型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E四种短周期元素的原子序数逐渐增大。A为非金属元素,且A、E同主族,C、D为同周期的相邻元素。E原子的质子数等于C、D原子最外层电子数之和。B原子最外层电子数是内层电子数的2倍。C的氢化物分子中有3个共价键,试推断:
(1)写出B元素在周期表中的位置____________________;
(2)由A、C、D所形成的离子化合物是_______________(填化学式),所含化学键类型为_____________,它与E的最高价氧化物对应水化物的溶液加热时反应的离子方程式是___________________________。
(3) C单质的电子式为____________________。
(4) B和D相比,非金属性较强的是_________________(用元素符号表示),下列事实能证明这一结论的是________________(选填字母序号)。
a.常温下,B的单质呈固态,D的单质呈气态 b.D的氢化物的稳定性强于B的氢化物
c.B与D形成的化合物中,B呈正价 d.D的氢化物的沸点高于B的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于四个图象的说法正确的是( ) 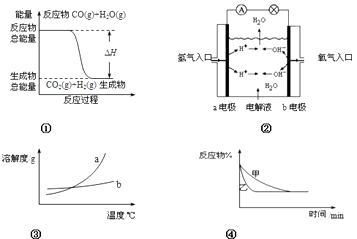
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H>0
B.图②为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯a
D.图④可以表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,且乙的压强大
3C(g)+D(s)的影响,且乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2(g)+3H2(g)2NH3(g)在密闭容器中进行.下列关于该反应的说法正确的是( )
A.加热能减慢反应速率
B.增大压强能加快反应速率
C.反应达到平衡时,v(正反应)=v(逆反应)=0
D.反应达到平衡时,N2转化率为100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com