
| 试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ① | 取少量该焰火原料加入冷水 | 无明显现象 | 不含Li、Na等活泼金属 |
| ② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体产生,溶液呈无色 | 可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种 |
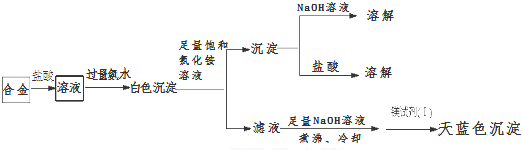

分析 (1)①Na、Li等活泼金属和与水反应;
②能与盐酸反应为较活泼的金属;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀;
(3)由题给信息可知Mg(OH)2可溶于浓的氯化铵溶液,应排除NH4+的干扰;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量;
②利用端值法判断;
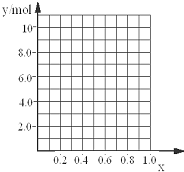
③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3.
解答 解:(1)①原料加入冷水无现象表明不含Li、Na等活泼金属,
故答案为;不含Li、Na等活泼金属;
②原料与盐酸反应产生气体表明含有能与盐酸反应的较活泼的金属,可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
故答案为:可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种;
(2)第②组实验所得的溶液含有过量盐酸,加入2滴NaOH溶液则不会产生沉淀,从而不能吸附镁试剂(I)染料呈天蓝色,由资料知,反应必须在碱性条件下进行;
故答案为:错误;由资料知,反应必须在碱性条件下进行;
(3)由图结合题意知该合金含镁、铝(不溶于足量饱和氯化铵溶液的白色沉淀既能溶液盐酸又能溶液氢氧化钠),由于Mg(OH)2可溶于浓的氯化铵溶液,因此用镁试剂(Ⅰ)染料检验Mg2+时要排除NH4+的干扰,所以滤液加入足量氢氧化钠溶液将NH4+转化为NH3,煮沸将氨气赶出,
故答案为:Mg和Al;将NH4+转化为NH3,煮沸促进氨气逸出,防止NH4+干扰Mg2+的检验;
(4)①镁和铝都能与盐酸反应生成氢气,根据氢气的体积结合合金总质量可确定合金的组成,加入过量氢氧化钠得到的沉淀为氢氧化镁,灼烧后可得到氧化镁,根据氧化镁的质量可知镁的质量,则可知铝的质量,已知镁的质量和镁铝生成氢气的体积可知铝的质量,则a、b、c都可测定合金的组成,
故答案为:a、b、c;
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,相对分子质量较小的为镁,如x=0,则全被为铝,7mol铝反应生成10.5mol氢气,如全被为镁,即x=7,则生成氢气7mol,则图象为 ,
,
故答案为: ;
;
③当y=8.5mol时,该合金是一种金属互化物,设合金中Mg为m mol,Al为n mol,则m+n=7 m+1.5n=8.5,解得m=4,n=3,
则化学式为Mg4Al3,
故答案为:Mg4Al3.
点评 本题考查物质含量的测定,侧重于考查学生的实验能力和分析能力,注意根据物质的性质进行判断,题目难度较大.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶液中存在电离平衡:(NH4)2SO4?2NH4++SO42- | |
| B. | 向溶液中滴加少量浓硫酸,c(NH4+)与c(SO42-)均增大 | |
| C. | 加水稀释,溶液中所有离子的浓度均减小 | |
| D. | 溶液中:c(SO42-)=2c(NH4+)+2c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的物质的量浓度不再改变 | |
| B. | 混合气的密度不再随时间而变化 | |
| C. | 容器内的压强不随时间而变化 | |
| D. | 平衡混合气体的平均相对分子质量不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na3PO4 | B. | Na3PO3 | ||
| C. | Na4P2O7 和Na5P3O10 | D. | Na3PO4、Na4P2O7和Na5P3O10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com