
ԭ������������������ֶ�����Ԫ��X��Y��Z��Q��R����֪X��Qͬ���壬Y��Zԭ������֮��Ϊ3��4��Z��������������Q��������������6����RΪͬ������ԭ�Ӱ뾶��С��Ԫ��(ϡ������Ԫ�س���)��X��R�γɵĻ����ﳣ����Ϊ��̬��
��1����ʾYԪ��������������������ȵ�ͬλ�ط����� ��
��2��Q��Z�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ĵ���ʽ�� ��
��3��A+B��C+D+H2OΪ��ѧ��ѧ�г����ķ�Ӧ��ʽ��A��B��C��D��Ϊ����������Ԫ����ɵĵ��ʻ��
����AΪNaOH��BΪCO2ʱ����д��aNaOH + bCO2 = cNa2CO3 + d NaHCO3 + nH2O��a��b�����ʵ���֮��Ӧ����Ĺ�ϵ�� ������l00 mL��3 mol��L��NaOH��Һ�л���ͨ���״����4��48 L��CO2���壬��l����ѧ����ʽ��ʾ���Ϸ�Ӧ
(��ѧ������Ϊ�������)����ʱ��Һ�и����������ʵ���Ũ���ɸߵ��͵�����˳����_ _��
������дһ������A+B��C+D+H2O��ʽ��������ԭ��Ӧ����ʽ������C��D��Ϊ��
��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
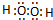
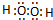
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
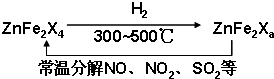
| a |
| Vd-a |
| 1000a |
| 35V |
| 1000b |
| V |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com