
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| V(标准)×c(标准) |
| V(待测) |
| (20.50-0.40)+(24.00-4.10) |
| 2 |
| V(标准)×c(标准) |
| V(待测) |
| 0.1000mol/L×20.00mL |
| 10.00mL |


科目:高中化学 来源: 题型:
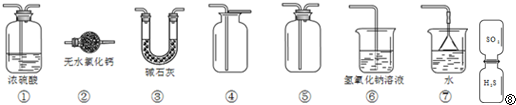
| 通电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
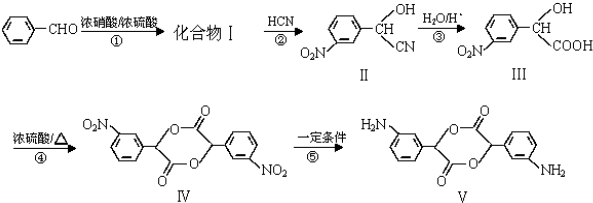
| 一定条件 |
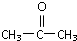 )代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为
)代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
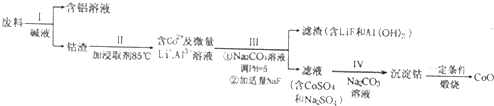
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、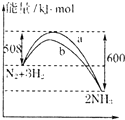 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 |
B、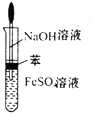 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 |
C、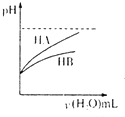 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB |
D、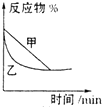 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
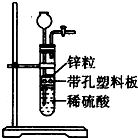 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )| A、①②③ | B、②④⑤ |
| C、①②④⑥ | D、②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
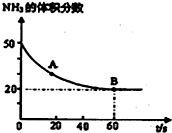 氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.
氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com