
下列表示对应化学反应的离子方程式正确的是( )
A.NO2通入水中:3NO2+H2O===2H++2NO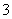 +NO
+NO
B.用两个铜电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
C.SO2通入FeCl3溶液中:SO2+Fe3++2H2O===SO +Fe2++4H+
+Fe2++4H+
D.过量的CO2通入NaAlO2溶液中:2AlO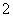 +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO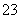
科目:高中化学 来源: 题型:
在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO +16H++5Na2O2===2Mn2++5O2↑+8H2O+10Na+。下列判断正确的是( )
+16H++5Na2O2===2Mn2++5O2↑+8H2O+10Na+。下列判断正确的是( )
A.Na2O2既是氧化剂,又是还原剂
B.O2是还原产物,Mn2+是氧化产物
C.通常用浓盐酸酸化高锰酸钾溶液
D.标准状况下,产生22.4 L O2时反应转移2 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图装置进行实验(A为电流计):
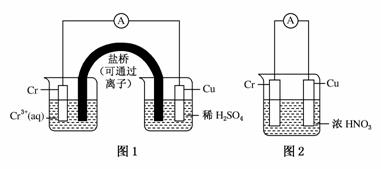
观察到现象:
装置图1:Cu电极上产生大量的无色气泡
装置图2:Cu电极上无气泡产生,而Cr电极上产生大量气泡
则下列说法正确的是( )
A.图1是电解池,图2是原电池
B.两个电池中,电子均由Cr电极流向Cu电极
C.图2中Cr电极可能被浓HNO3钝化成惰性电极
D.由实验现象可知金属活动性:Cu>Cr
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
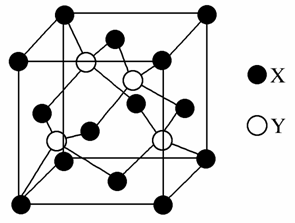
①在1个晶胞中,X离子的数目为________。
②该化合物的化学式为________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是______________________________________________________________。
(4)Y与Z可形成YZ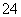 。
。
①YZ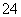 的空间构型为________(用文字描述)。
的空间构型为________(用文字描述)。
②写出一种与YZ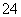 互为等电子体的分子的化学式:________。
互为等电子体的分子的化学式:________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
[已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7]

(金属离子含量与混合液pH、CuCl产率与混合液pH的关系图)
请回答下列问题:
(1)酸浸时发生反应的离子方程式是______________________;析出CuCl晶体时的最佳pH在____左右。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为________________________________________________________________________。
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70 ℃干燥2小时、冷却,密封包装。70 ℃真空干燥、密封包装的目的是_____________________________________________________________。
(4)产品滤出时所得滤液的主要成分是________________,若想从滤液中获取FeSO4·7H2O晶体,我们还需要知道的是_____________________。
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式________________________________________________。为提高CuCl的产率,常在该反应体系中加入稀碱溶液,调节pH至3.5。这样做的目的是__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下下列各组离子在给定条件下一定能大量共存的是( )
A.水电离出的c(H+)=1×10-14 mol·L-1的溶液:K+、AlO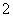 、Br-、Cl-
、Br-、Cl-
B.在含有Al3+、Cl-的溶液中:HCO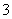 、I-、NH
、I-、NH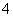 、Mg2+
、Mg2+
C.在c(H+)=1×10-13 mol·L-1的溶液中:Na+、S2-、SO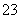 、NO
、NO
D.在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C.乙醇和乙酸都能发生氧化反应
D.乙醇与乙酸反应生成乙酸乙酯,说明乙醇具有碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
例海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:
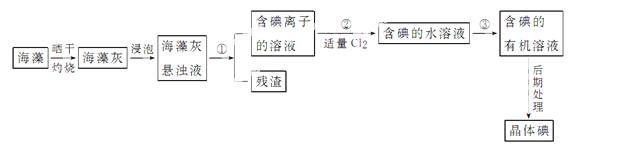
(1)指出提取碘的过程中有关的实验操作名称:① ,③ ;写出实验②中有关反应的离子方程式_______。
(2)提取碘的过程中,可供选择的有关试剂是 。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)从海藻灰中碘离子转化到碘的有机溶液,实验室准备了烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品。如右图所示,还缺少的玻璃仪器是________。
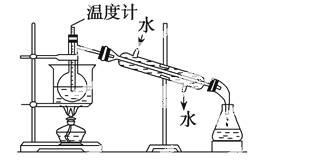
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出上图实验装置中的错误之处:①_______, ② ,③ 。
(5)进行上述蒸馏操作时,使用水浴的原因是 ;最后,晶体碘在 里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列 说法错误的是
说法错误的是
A.石油的炼制过程不都是化学变化
B.煤是工业上获得芳香烃的一种重要原料
C.石油经过常、减压分馏及裂化等工序炼制后即能得到纯净物
D.煤通过液化和气化处理能减少环境污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com